
�����й�Fe2(SO4)3��Һ��������ȷ����
A������Һ��K����Fe2����C6H5OH��Br�����Դ�������
B����KI��Һ��Ӧ�����ӷ���ʽ��Fe3����2I����Fe2����I2
C����Ba(OH)2��Һ��Ӧ�����ӷ��� ʽ��Fe3����SO42—��Ba2����3OH����Fe(OH)3����Ba SO4��
ʽ��Fe3����SO42—��Ba2����3OH����Fe(OH)3����Ba SO4��
D��1 L0.1 mol·L—1����Һ��������Zn��ַ�Ӧ������11.2 g Fe

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���Ǵ����к����ḻ��һ��Ԫ�أ������仯������������������������Ҫ���ã����ٵ���������ŷ��ǻ�����������Ҫ����֮һ����ش����е����仯�����������⣺
��1���ݱ������������ѧ�һ���˼����о���ֵ��N4������ӽṹ������ӵ���������ṹ���ƣ���֪����1mol N��N������167kJ����������1mol N��N���ų�942kJ��������д��N4����ת��ΪN2��Ӧ���Ȼ�ѧ����ʽ����N4��g��=2N2��g������H=��882kJ/mol����
��2���ݱ�����NH3��ֱ����������ȼ�ϵ�أ�д���õ�صĸ�����Ӧʽ����2NH3+6OH����6e��=N2+6H2O����
��3����T1��ʱ����5mol N2O5����10L�̶��ݻ����ܱ������з������з�Ӧ��2N2O5��g��⇌4NO2��g��+O2��g������H��0����Ӧ��5����ʱ�����ʵ�Ũ�Ȳ��ٷ����仯�����NO2���������Ϊ50%��
����÷�Ӧ��ƽ�ⳣ��K=��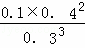 �������ִ���ʽ�Ӽ��ɣ�������ƽ����ϵ��O2���������Ϊ��12.5%����
�������ִ���ʽ�Ӽ��ɣ�������ƽ����ϵ��O2���������Ϊ��12.5%����
����O2��ʾ��0��5min�ڸ÷�Ӧ��ƽ�����ʦԣ�O2��=��0.02mol/��L•min������
�۽�����ƽ����ϵ���¶Ƚ���T2�棬�ܱ������ڼ�С���������С�AC����
A��ѹǿ B���ܶ� C����Ӧ���� D��N2O5��Ũ��
��4���ں��º��ݵ��ܱ������г���NO2����������ƽ�⣺2NO2��g��⇌N2O4��g����ƽ��ʱN2O4��NO2�����ʵ���֮��Ϊa�������������������£��ֱ��ٳ���NO2���ٳ���N2O4��ƽ�������ı仯��ȷ���ǡ�B����
A��������a��С
B��������a����
C������NO2����a��������N2O4����a����
D������NO2����a������N2O4����a����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ����ȷ����(����)
A������ʯ��ˮ��ϡ���ᷴӦCa(OH)2��2H��===Ca2���� 2H2O
2H2O
B���������������ᷴӦOH����H��===H2O
C��ͭƬ������������Һ��Cu��Ag��===Cu2����Ag
D���Ȼ�þ��Һ������������Һ��ӦMg2����2OH��===Mg(OH)2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ�п��ܺ���Na+��NH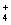 ��Ba2+��SO
��Ba2+��SO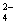 ��I����S2�����ֱ�ȡ��������pH�Ʋ��ԣ���Һ�������ԣ��ڼ���ˮ�͵�������������Ϊȷ������Һ����ɣ���������������
��I����S2�����ֱ�ȡ��������pH�Ʋ��ԣ���Һ�������ԣ��ڼ���ˮ�͵�������������Ϊȷ������Һ����ɣ���������������
A�� Na+ B��SO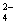 C�� Ba2+ D��NH
C�� Ba2+ D��NH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ˮ��Һ���ܴ��������һ�������ǣ�������
A��Fe2+��Al3+��ClO﹣��Cl﹣ B��K+��Cu2+��OH﹣��NO3﹣
C��NH4+��Na+��Br﹣��SO42﹣ D��Mg2+��H+��SiO32﹣��SO42﹣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����б仯�ٴ����̵��ڳ��ȵ�̼��ŨHNO3��Ӧ��ʵ������ȡ�����У�����Ԫ�ر�����������ԭ���Ȳ��������ֲ�����ԭ��˳�����У���ȷ����(����)
A���٢ڢ� B���ڢ٢�
C���ۢڢ� D���ۢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������з���ʽ����2Fe2++Cl2=2Fe3++2Cl- ����HClO+HCl=Cl2+H2O ����2Fe3����Cu=2Fe2++Cu2+����Fe+Cu2+=Fe2++Cu���ж����� ��������������ǿ��˳����ȷ����
��������������ǿ��˳����ȷ����
A��Fe3+�� HClO��Cl2��Fe2+��Cu2+ B��HClO��Cl2��Fe3+��Cu2+��Fe2+
HClO��Cl2��Fe2+��Cu2+ B��HClO��Cl2��Fe3+��Cu2+��Fe2+
C��Cl2��HClO��Fe3+��Cu2+��Fe2+ 
 D��HClO��Fe3+��Cl2
D��HClO��Fe3+��Cl2 ��Cu2+��Fe2+
��Cu2+��Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л����� �������з����ķ�Ӧ������������ԭ��Ӧ����
�������з����ķ�Ӧ������������ԭ��Ӧ����
A����������Ư�� B����ʯ��ʯ����ʯ��
C����±ˮ����ȡ�嵥�� D���ð���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ר�Ҷ�ʯ�ҵ����½����������о�����Ҳʹ��ʯ�ҵ���һ���ϵķ����ֻ������µĻ�����ʯ�ҵ�����Ca��N��C������Ԫ����ɵ��Σ��京�ơ��������������ֱ�Ϊ50 %��35%��ʯ�ҵ���ȫˮ���IJ����ǹ���A������B������B����ȡ���ʵ���Ҫԭ�ϡ�����A�ڸ����·ֽ�����D������C��B�Ĵ���������ΪE��F��F����������IJ���G����E����һ�ֹ�ҵǿ�ᡣ��G��F�Ļ�����ܽ��ڽӽ���ȵ�ˮ�У��������������ˮ��Һ���÷�Ӧ�ɱ�ʾ����G+F+H2O��2HNO2������ƽ������ش��������⣺
%��35%��ʯ�ҵ���ȫˮ���IJ����ǹ���A������B������B����ȡ���ʵ���Ҫԭ�ϡ�����A�ڸ����·ֽ�����D������C��B�Ĵ���������ΪE��F��F����������IJ���G����E����һ�ֹ�ҵǿ�ᡣ��G��F�Ļ�����ܽ��ڽӽ���ȵ�ˮ�У��������������ˮ��Һ���÷�Ӧ�ɱ�ʾ����G+F+H2O��2HNO2������ƽ������ش��������⣺
��1��ʯ�ҵ��Ļ�ѧʽΪ �� ��
��2������B��C�뱥���� ������Һ�ķ�Ӧ�ǻ�������������ij����Ҫ������Ʒ����Ҫ��Ӧ����д���仯ѧ����ʽ
������Һ�ķ�Ӧ�ǻ�������������ij����Ҫ������Ʒ����Ҫ��Ӧ����д���仯ѧ����ʽ  ��
��
��3�������ᣨHNO2����һ������������൱�����ᣬ�ܲ��ȶ���ͨ���������������ֽ⡣�����������£���NaNO2��KI�����ʵ���1��1ǡ����ȫ��Ӧ����I— ������ΪI2ʱ����������Ϊ ���ѧʽ����Ҫ�õ��ȶ�HNO2��Һ���������䶳��ŨNaNO2��Һ�м����ͨ��ij�����ʣ����������в��ʺ�ʹ���� �� ������ţ���
a������ b��������̼ c��ϡ���� d���������� e��������
��4����ҵ��ˮ�е�NO2— �������۳�ȥ����֪�˷�Ӧ��ϵ�а���Al��NaAlO2��NaNO2��NaOH��NH3��H2O�������ʡ�д��������Ӧ�����ӷ���ʽ�� ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com