
判断一个化学反应的自发性常用焓判据和熵判据,则在下列情况下,可以判定反应一定自发进行的是( )
| A.ΔH>0,ΔS>0 | B.ΔH<0,ΔS<0 |
| C.ΔH>0,ΔS<0 | D.ΔH<0,ΔS>0 |
科目:高中化学 来源: 题型:单选题
已知298K时,2SO2(g)+O2(g)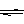 2SO3(g);△H=-197KJ/mol。在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1,向另一个体积相同的容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出热量Q2。则下列关系式正确的是( )
2SO3(g);△H=-197KJ/mol。在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1,向另一个体积相同的容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出热量Q2。则下列关系式正确的是( )
| A.Q1=Q2=197KJ | B.Q1<Q2<197KJ | C.Q2<Q1<197KJ | D.Q1=Q2<197KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知某温度下,在2L密闭容器中加入一定量A,发生以下化学反应:2A(g) 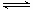 B(g) + C(g);ΔH = ?48.25 kJ/L
B(g) + C(g);ΔH = ?48.25 kJ/L
时间t与A 、B的浓度有下图所示关系,若测得第15min时c(B)=1.6 mol/L,则下列结论正确的是( )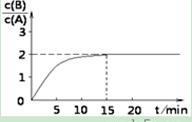
A.该温度下此反应平衡常数为3.2
B.A的初始物质的量为4 mol
C.0-15min内,气体密度不变
D.要使c(B)/c(A)= 3,只能降低反应温度
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一密闭容器中,等物质的量的A和B发生反应:A(g)+2B(g) 2C(g),反应达平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )
2C(g),反应达平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )
| A.40% | B.50% | C.60% | D.70% |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组实验中溶液最先变浑浊的是( )
| A.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B.0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度30℃ |
| D.0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图表示外界条件(温度、压力)的变化对下列反应的影响:L(s)+G(g) 2R(g) ΔH>0。在图中Y轴是指
2R(g) ΔH>0。在图中Y轴是指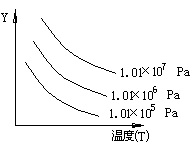
| A.平衡混合气中R的质量分数 | B.G的转化率 |
| C.平衡混合气中G的体积分数 | D.L的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于反应C(s)+H2O(g)  CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
A.平衡常数表达式为K=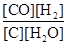 |
| B.增大体系压强,平衡常数K不发生变化 |
| C.升高体系温度,平衡常数K减小 |
| D.增加C(s)的量,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某恒温密闭容器中,可逆反应A(s)  B+C(g) ΔH="Q" kJ·mol-1(Q>0 ),达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是
B+C(g) ΔH="Q" kJ·mol-1(Q>0 ),达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是
| A.产物B的状态可能为固态或液态 |
| B.平衡时,单位时间内A和B消耗的物质的量之比为1:1 |
| C.保持体积不变,向平衡体系中加入A(s),平衡不移动 |
| D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
取五等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)  N2O4(g) ΔH<0 反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是
N2O4(g) ΔH<0 反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是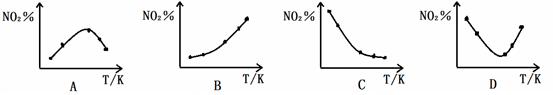
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com