
| A. | 108g | B. | 54g | C. | 216g | D. | 64g |
分析 相同条件下,通过相同的电量分别电解CuCl2和AgNO3溶液,电解过程中转移的电子数一定相等,根据n=$\frac{m}{M}$计算出64gCu的物质的量,再根据电子守恒计算出生成银的物质的量,最后根据m=nM计算出析出Ag的质量.
解答 解:相同条件下,通过相同的电量分别电解CuCl2和AgNO3溶液,则电解过程中转移电子的物质的量相同,
64gCu的物质的量为:$\frac{64g}{64g/mol}$=1mol,生成1molCu得到电子的物质的量为:1mol×2=2mol,
则转移2mol电子时生成Ag的物质的量为:$\frac{2mol}{1}$=2mol,
所以析出Ag的质量为:108g/mol×2=216g,
故选C.
点评 本题考查了电解原理及其应用,题目难度中等,明确电解原理为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.8g | B. | 4.2g | C. | 8.4g | D. | 11.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若所得溶液呈中性,则生成的盐可能为强酸强碱盐 | |
| B. | 若所得溶液呈碱性,则一定是强碱与弱酸溶液反应 | |
| C. | 若所得溶液呈酸性,则可能是弱酸与强碱溶液反应 | |
| D. | 若所得溶液的pH=9,则水电离产生的c(OH-)可能为10-9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=1 | |
| B. | B的转化率为20% | |
| C. | 反应的10s内A的反应速率为0.3mol•L-1•s-1 | |
| D. | 反应进行到10s时,在相同温度下容器内混合气体的压强是反应前的85% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
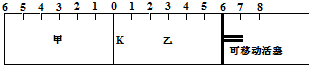
| A. | 右侧6处 | B. | 右侧6~7处 | C. | 右侧7处 | D. | 右侧7~8处 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com