
【题目】肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4![]() H2O):
H2O):![]()
NaClO过量时,易发生反应:![]()
实验一:制备NaClO溶液(实验装置如图甲所示)

锥形瓶中发生反应的离子方程式是__________________。
实验二:制取水合肼(实验装置如图乙所示)

控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108-114℃馏分。
分液漏斗中的溶液是_____________(填序号);
A、CO(NH2)2溶液 B、NaOH溶液 C、NaOH和CO(NH2)2混合溶液 D、NaOH和NaClO混合溶液
选择的理由是_________________。
实验三:测定馏分中肼含量
称取馏分5.000g加入适量NaHCO3固体,加入配成250mL溶液,移出25.00mL,用0.1000mol/L的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右(已知:N2H4![]() H2O+2I2═N2↑+4HI+H2O)。
H2O+2I2═N2↑+4HI+H2O)。
配制250mL溶液所需仪器除分析天平、烧杯、玻璃棒外,还需______________。
滴定过程中,NaHCO3能控制溶液的pH在6.5左右,用离子方程式解释其原因:__________。
实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4![]() H2O)的质量分数为____________。
H2O)的质量分数为____________。
【答案】Cl2+2OH-=Cl-+ClO-+H2OD如果次氯酸钠装在烧瓶中,因过量而使N2H4![]() H2O氯化250mL容量瓶,胶头滴管HCO3-+H+═H2O+CO2↑10%
H2O氯化250mL容量瓶,胶头滴管HCO3-+H+═H2O+CO2↑10%
【解析】实验一:氯气与氢氧化钠溶液反应的离子方程式为Cl2+ 2OH—=ClO— + Cl— + H2O;
实验二:由于水合肼易被次氯酸钠氧化,因此如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化,所以分液漏斗中的溶液是NaOH和NaClO混合溶液,答案选D;理由为:如果次氯酸钠溶液装在烧瓶中,因过量而使水合肼被氧化;
实验三:配制溶液需要用天平称量固体,需要在烧杯内溶解固体,需要用量筒最取水,用玻璃棒搅拌,还用到胶头滴管,故除所需仪器除分析天平、烧杯、玻璃棒外,还需要250mL容量瓶,胶头滴管;生成的氢碘酸是强酸,能与次氯酸钠溶液反应,从而可以控制溶液的pH值,用离子方程式解释:HCO3-+H+= H2O+CO2↑;消耗碘的物质的量是0.1000mol/L ×0.020L=0.002mol,则水合肼的物质的量是0.001mol,质量是0.001mol×50g/mol=0.05g,则馏分中水合肼(N2H4·H2O)的质量分数为:![]() 。
。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为HOOC—CH=CH-CH2OH。
回答下列问题:
(1)请你写出该有机物所含有的官能团的名称:__________________。
(2)验证该有机物中含有-COOH官能团常采用的方法和现象:_____________________。
(3)写出该有机物与溴水反应的化学方程式:_________,反应类型为______。
(4)该有机物可与乙醇发生酯化反应,写出该反应的方程式:____________________,请你写出能增大该反应反应速率的一条措施:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式正确的是
A. 向Na2SiO3溶液中通入过量CO2:SiO32-+ CO2+ H2O= H2SiO3(胶体)+ CO32-
B. 用醋酸溶液除水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
C. 向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2![]() 2CO2+2CaSO4
2CO2+2CaSO4
D. 碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀:CO32﹣+Ca2+=CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于离子反应的是( )
A.H2和O2的反应
B.铁与CuSO4溶液的反应
C.Ba(OH)2溶液和H2SO4溶液的反应
D.Zn和稀H2SO4反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列烷烃的表示式:
分子中含有34个氢原子化学式_________。分子中有26个电子的结构简式_________。 支链含乙基的烷烃中相对分子质量最小的物质名称是_______________。
(2)现有A、B、C三种烃,其球棍模型下图:

①等质量的以上物质完全燃烧时耗去O2的量最多的是______(填对应字母,下同);
②同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是______;
③在120℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下,下列物质按沸点升高的顺序排列正确的是 ( )。
① 辛烷 ② 十四烷 ③壬烷 ④ 丙烷
A. ②③①④ B. ④①③② C. ①②③④ D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中Cl元素全部被氧化的是
A.KClO3+6HCl=KCl+3Cl2↑+3H2O
B.2NaCl电解2Na+Cl2↑
C.H2+Cl2光照2HCl
D.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常教,下列叔述正确的是( )
A. 常温常压下,9.2gNO2气体中.分子数为0.2NA
B. pH=2的硫酸溶液中,H+数目为0.01NA
C. 将0.05molFeCl3全部转化为Fe(OH)3胶体,则胶粒数目为0.05NA
D. 20gD2O中含有的质子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是________________________
(2)如图是某温度下,N2与H2反应过程中能量变化的曲线图。
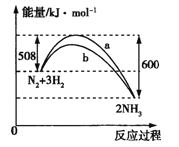
a、b两条曲线产生区别的原因很可能是________________。
(3)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol H2O(l)时放出571.6 kJ热量,则H2的热值为________
(4)已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g) ΔH=489.0 kJ·mol-1
CO(g)+![]() O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
由Fe(s)和O2(g)反应生成Fe2O3(s)的热化学方程式为_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com