
øł¾ŻĻĀĶ¼ŗ£Ė®×ŪŗĻĄūÓĆµÄ¹¤ŅµĮ÷³ĢĶ¼£¬ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
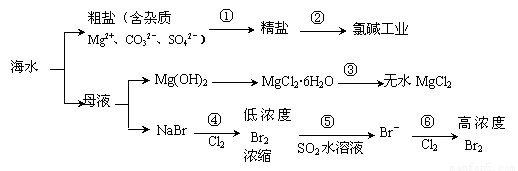
A£®¹ż³Ģ¢ŁµÄĢį“æŹĒĪļĄķ¹ż³Ģ£¬¹ż³Ģ¢ŚĶعżŃõ»Æ»¹Ō·“Ó¦æɲśÉś2ÖÖµ„ÖŹ
B£®³żČ„“ÖŃĪÖŠµÄSO42-”¢Ca2+”¢Mg2+”¢Fe3+µČŌÓÖŹ£¬¼ÓČėµÄŅ©Ę·Ė³ŠņĪŖ£ŗNa2CO3ČÜŅŗ”śNaOHČÜŅŗ”śBaCl2ČÜŅŗ”ś¹żĀĖŗó¼ÓŃĪĖį
C£®ŌŚ¹ż³Ģ¢ŪÖŠ½«MgCl2”¤6H2O×ĘÉÕ¼“æÉÖʵĆĪŽĖ®MgCl2
D£®ŌŚ¹ż³Ģ¢Ü”¢¢Ž·“Ó¦ÖŠĆæŃõ»Æ0.2 mol Br£ŠčĻūŗÄ0.1mol Cl2

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗž±±ŗ½ĢģøßÖŠ”¢°²Ā½¶žÖŠµČĪ劣øßŅ»ÉĻĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŗÓĻŗ²»ŅĖÓėĪ÷ŗģŹĮĶ¬Ź³£¬Ö÷ŅŖŌŅņŹĒŗÓĻŗÖŠŗ¬+5¼ŪÉ飬Ī÷ŗģŹĮÖŠŗ¬ÓŠ½Ļ¶ąµÄĪ¬ÉśĖŲC£¬Į½ÕßĶ¬Ź³»į²śÉśÓŠ¶¾µÄ+3¼ŪÉ飮¾Ż“Ė£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®øĆ·“Ó¦ÖŠĪ¬ÉśĖŲC×÷»¹Ō¼Į
B£®øĆ·“Ó¦ÖŠÉéŌŖĖŲ±»Ńõ»Æ
C£®ŗÓĻŗÓėĪ÷ŗģŹĮĶ¬Ź³·¢ÉśĮĖŃõ»Æ»¹Ō·“Ó¦
D£®ŗÓĻŗÓėĘäĖüŗ¬Ī¬ÉśĖŲC½Ļ¶ąŹß²ĖŅ²²»ŅĖĶ¬Ź³
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶žÉĻѧʌ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ²»Ķ¬ÅØ¶Č£Øc£©”¢ĪĀ¶Č£ØT£©Ģõ¼žĻĀ£¬ÕįĢĒĖ®½āµÄĖ²Ź±ĖŁĀŹ£Øv£©ČēĻĀ±ķ£®ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ
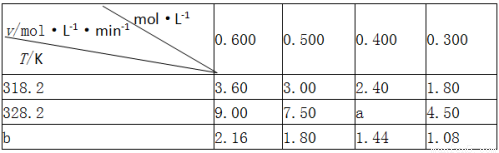
A£® a=6.00
B£® Ķ¬Ź±øı䷓ӦĪĀ¶ČŗĶÕįĢĒµÄÅØ¶Č£¬væÉÄܲ»±ä
C£® b£¼318.2
D£® ²»Ķ¬ĪĀ¶ČŹ±£¬ÕįĢĒÅØ¶Č¼õÉŁŅ»°ėĖłŠčµÄŹ±¼äĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģĮÉÄžŹ”øßČżÉĻѧʌµŚ¶ž“ĪÄ£Äā²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖĻĀ±ķŹż¾Ż£ŗ
ĪļÖŹ | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25”ćC) | 8.0”Į10-16 | 2.2”Į10-20 | 4.0”Į10-38 |
ĶźČ«³ĮµķŹ±PH·¶Ī§ | ”Ż9.6 | ”Ż6.4 | ”Ż3.4 |
¶Ōŗ¬µČĪļÖŹµÄĮæµÄCuSO4”¢FeSO4”¢Fe2(SO4)3µÄ»ģŗĻČÜŅŗµÄĖµ·Ø£¬²»ÕżČ·µÄŹĒ
A£®ĻņøĆ»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ£¬×īĻČ擵½ŗģŗÖÉ«³Įµķ
B£®øĆČÜŅŗÖŠc(SO42-)£ŗ[c(Cu2+)+c(Fe2+)+c(Fe3+)]> 5£ŗ4
C£®ĻņøĆČÜŅŗÖŠ¼ÓČėŹŹĮæĀČĖ®£¬²¢µ÷½ŚpHµ½3”Ŗ4ŗó¹żĀĖ£¬æÉ»ńµĆ“æ¾»µÄCuSO4ČÜŅŗ
D£®ŌŚpH=5µÄČÜŅŗÖŠFe3+²»ÄÜ“óĮæ“ęŌŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģɽ¶«Ź”øßČżÉĻѧʌʌ֊²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĶʶĻÕżČ·µÄŹĒ
A£®SiO2 ŹĒĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ó¦
B£®Na2O”¢Na2O2×é³ÉŌŖĖŲĻąĶ¬£¬Óė CO2·“Ó¦²śĪļŅ²ĻąĶ¬
C£®CO”¢NO”¢NO2¶¼ŹĒ“óĘųĪŪČ¾ĘųĢ壬ŌŚæÕĘųÖŠ¶¼ÄÜĪČ¶Ø“ęŌŚ
D£®ŠĀÖĘĀČĖ®ĻŌĖįŠŌ£¬ĻņĘäÖŠµĪ¼ÓÉŁĮæ×ĻÉ«ŹÆČļŹŌŅŗ£¬³ä·ÖÕńµ“ŗóČÜŅŗ³ŹŗģÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹµŃé֊ѧø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŹŅĪĀĻĀ£¬ĻĀĮŠČÜŅŗÖŠµÄĪ¢Į£ÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ£Ø £©
A£®ŠĀÖĘĀČĖ®ÖŠ¼ÓČė¹ĢĢåNAOH£ŗC(NA£«)£½C(Cl£)£«C(ClO£)£«C(OH£)
B£®pH£½8.3µÄNAHCO3ČÜŅŗ£ŗC(NA£«)>C(HCO3-)>C(CO32£)>C(H2CO3)
C£®NA2CO3ČÜŅŗ£ŗC(NA£«)£«C(H£«)£½2C(CO32£)£«C(OH£)
D£®0.2 mol/L CH3COOHČÜŅŗÓė0.1 mol/L NAOHČÜŅŗµČĢå»ż»ģŗĻ£ŗ
2 C(NA£«)= C(CH3COO£)+C(CH3COOH)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«ÉĒĶ·½šÉ½ÖŠŃ§øßŅ»10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČŻĮæĘæŹĒÓĆĄ“ÅäÖĘĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗµÄ¶ØĮæŅĒĘ÷£¬ĘäÉĻ±źÓŠ£ŗ¢ŁĪĀ¶Č”¢¢ŚÅØ¶Č”¢¢ŪČŻĮ攢¢ÜŃ¹Ē攢¢ŻæĢ¶ČĻß”¢¢ŽĖįŹ½»ņ¼īŹ½ÕāĮłĻīÖŠµÄ
A£®¢Ś¢Ü¢Ž B£®¢Ū¢Ż¢Ž C£®¢Ł¢Ś¢Ü D£®¢Ł¢Ū¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ŗÓ±±ŹÆ¼Ņ×ƵŚŅ»ÖŠŃ§ø߶žÉĻĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŌŚ4000C£¬101.3k PaŹ±£¬3 LijĢžAŌŚm LŃõĘųÖŠĶźČ«Č¼ÉÕ£¬Č¼ÉÕŗó²āµĆĘųĢåĢå»ż£Øm+6£©L£ØĘųĢåĢå»ż¾łŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ²ā¶Ø£©ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĢžAµÄ×é³ÉÖŠÓ¦Āś×ćµÄĢõ¼ž £»
£Ø2£©µ±m=27Ź±£¬ĢžAæÉÄܵķÖ×ÓŹ½£ØÖ»ŅŖĒ󊓳öČżÖÖæÉÄܵķÖ×ÓŹ½£©”£ČżÖÖæÉÄܵķÖ×ÓŹ½ŹĒ£ŗ £¬ £¬ £»
£Ø3£©ČōĢžAŌŚ³£ĪĀ³£Ń¹ĻĀĪŖĘųĢ¬ĪļÖŹŹ±£¬mµÄȔֵ·¶Ī§ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗžÄĻŹ”ÖźÖŽŹŠøßČżÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¹āĘ×ŃŠ¾æ±ķĆ÷£¬Ņ×ČÜÓŚĖ®µÄSO2ĖłŠĪ³ÉµÄČÜŅŗÖŠ“ęŌŚ×ÅĻĀĮŠĘ½ŗā£ŗ
¾Ż“Ė£¬ĻĀĮŠÅŠ¶ĻÖŠÕżČ·µÄŹĒ
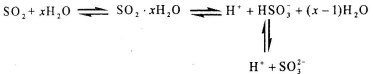
A£®øĆČÜŅŗÖŠ“ęŌŚ×ÅSO2·Ö×Ó
B£®øĆČÜŅŗÖŠH+ÅØ¶ČŹĒSO32£ÅØ¶ČµÄ2±¶
C£®ĻņøĆČÜŅŗÖŠ¼ÓČė×ćĮæµÄĖį¶¼ÄܷųöSO2ĘųĢå
D£®ĻņøĆČÜŅŗÖŠ¼ÓČė¹żĮæNaOHæɵƵ½Na2SO3 ”¢NaHSO3ŗĶNaOHµÄ»ģŗĻČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com