
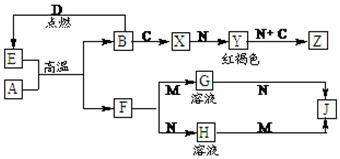
科目:高中化学 来源:不详 题型:单选题
| A.14 | B.31 | C.74.9 | D.121.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:As>C1>P | B.热稳定性:HC1>AsH3>HBr |
| C.还原性:As3->S2->C1- | D.酸性:H3AsO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.42He原子核内含有2个质子 |
| B.32He和42He互为同位素 |
| C.32He原子核内含有1个中子 |
| D.42He的最外层电子数为2,所以42He具有较强的金属性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
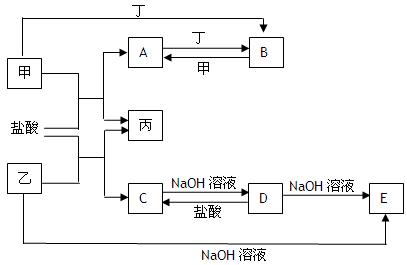
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 应条件略去)。
应条件略去)。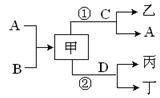
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
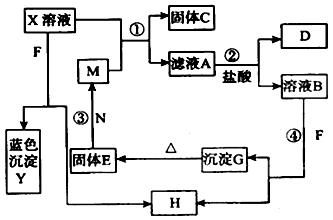
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子半径:Na+>N3->H+ | B.加热熔化时,都只破坏离子键 |
| C.与盐酸反应都只生成一种盐 | D.与水反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 中充分燃烧所得氧化物的电子式________________
中充分燃烧所得氧化物的电子式________________ 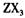 的浓溶液,现象为______________ ,
的浓溶液,现象为______________ ,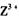 基态离子的电子排布式为
基态离子的电子排布式为 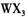 溶液为原料制取无水
溶液为原料制取无水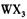 ,主要操作包括加热浓缩、冷却结晶、过滤,先制得
,主要操作包括加热浓缩、冷却结晶、过滤,先制得 晶体,然后在条件下加热
晶体,然后在条件下加热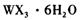 晶体,能进一步制取无水
晶体,能进一步制取无水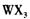 .其原因是(结合离子方程式简要说明) _____________________________________________
.其原因是(结合离子方程式简要说明) _____________________________________________查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com