
【题目】常温下,将NaOH固体分别加入浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,lg![]() 随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是( )
随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是( )
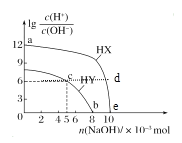
A.由a点到e点水的电离程度先增大后减小
B.d点溶液中存在:c(HX)+c(X-)=0.1mol/L
C.c点溶液中存在:c(Y-)+2c(OH-)=2c(H+)+c(HY)
D.b点溶液中存在:c(HY)+c(Na+)=0.1mol/L
【答案】CD
【解析】
A. a点lg![]() =12,则溶液中c(H+)=0.1mol/L,可知HX为强酸,e点lg
=12,则溶液中c(H+)=0.1mol/L,可知HX为强酸,e点lg![]() =0,则溶液中c(H+)=10-7mol/L完全中和,强酸对水的电离起抑制作用,酸的浓度减小,则水的电离变大,由a点到e点水的电离程度一直增大,A项错误;
=0,则溶液中c(H+)=10-7mol/L完全中和,强酸对水的电离起抑制作用,酸的浓度减小,则水的电离变大,由a点到e点水的电离程度一直增大,A项错误;
B. HX为强酸会完全电离,溶液中不存在HX,B项错误;
C. c点lg![]() =6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,根据电荷守恒有c(Y-)+c(OH-)=c(H+)+ c(Na+),根据元素守恒有c(Y-)+c(HY)=2c(Na+),联立两个等式可得c(Y-)+2c(OH-)=2c(H+)+c(HY),所以c(Y-)+2c(OH-)=2c(H+)+c(HY),C项正确;
=6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,根据电荷守恒有c(Y-)+c(OH-)=c(H+)+ c(Na+),根据元素守恒有c(Y-)+c(HY)=2c(Na+),联立两个等式可得c(Y-)+2c(OH-)=2c(H+)+c(HY),所以c(Y-)+2c(OH-)=2c(H+)+c(HY),C项正确;
D. b点lg![]() =0,则溶液中c(H+)=10-7mol/L= c(OH-),根据电荷守恒有c(Y-)+c(OH-)=c(H+)+ c(Na+),即c(Y-) = c(Na+),根据元素守恒有c(Y-)+c(HY)=0.1mol/L,联立两个等式可得c(HY)+c(Na+)=0.1mol/L,所以c(HY)+c(Na+)=0.1mol/L,D项正确;
=0,则溶液中c(H+)=10-7mol/L= c(OH-),根据电荷守恒有c(Y-)+c(OH-)=c(H+)+ c(Na+),即c(Y-) = c(Na+),根据元素守恒有c(Y-)+c(HY)=0.1mol/L,联立两个等式可得c(HY)+c(Na+)=0.1mol/L,所以c(HY)+c(Na+)=0.1mol/L,D项正确;
答案选CD。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种物质直接的转化如图所示,其中不能一步实现的是( )

A | B | C | D | |
X | C | NaOH | CH3CH2OH | N2 |
Y | CO | Na2CO3 | CH3CHO | NH3 |
Z | CO2 | NaHCO3 | CH3COOH | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2A(g)![]() B(g)+D(g),在四种不同条件下进行,投入反应物A,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g),在四种不同条件下进行,投入反应物A,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:

根据上述数据,完成下列填空:
(1)在实验1,反应在20至30分钟时间内平均速率为_____mol/(L·min)。
(2)在实验2,反应经20分钟就达到平衡的原因可能是______。A的初始浓度C2______1.0mol/L(填>、=、<)。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3____V1(填>、=、<),且C3___1.0mol/L(填>、=、<)。
(4)从实验4可推测该反应是____反应(选填“吸热”“放热”)。理由是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
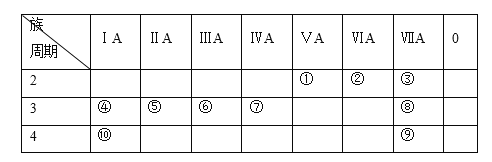
(1)10种元素中,化学性质最活泼的金属是________。
(2)④、⑤、⑥两种元素最高价氧化物对应的水化物中,碱性最强的是________。
(3)③、④两种元素形成的离子,离子半径由大到小的顺序是________。
(4)④和⑨两种元素形成化合物的化学式为________,该化合物燃烧时的焰色为________,该化合物溶液与元素⑧的单质反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。
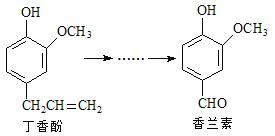
有关上述两种化合物的说法正确的是
A. 常温下,1mol丁香酚只能与1molBr2反应
B. 丁香酚不能使FeCl3溶液发生显色反应
C. 1mol香兰素最多能与3mol氢气发生加成反应
D. 香兰素分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2L的恒容密闭容器中发生反应xA(g)+yB(g) ![]() zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化,图2表示温度与C的体积分数的变化关系,则下列结论正确的是
zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化,图2表示温度与C的体积分数的变化关系,则下列结论正确的是
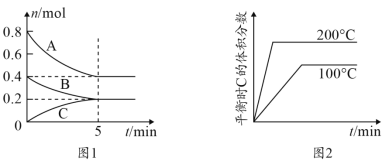
A.由图可知该反应为2A(g)+B(g) ![]() C(g) ΔH<0
C(g) ΔH<0
B.200℃,该反应的平衡常数为25
C.200℃时,反应从开始到平衡的平均速率v(B)=0.04mol·L-1·min-1
D.当外界条件由200℃降温到100℃,原平衡被破坏,且正逆反应速率均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下分别测得反应2SO2+O2![]() 2SO3的化学反应速率,其中表示该反应进行得最快的是( )
2SO3的化学反应速率,其中表示该反应进行得最快的是( )
A.v(SO2)=4mol/(L·min)B.v(O2)=3mol/(L·min)
C.v(SO2)=0.1mol/(L·s)D.v(O2)=0.1mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com