
【题目】用0.1molL﹣1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1molL﹣1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图: 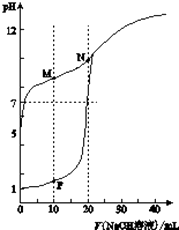
(1)HX为酸(填“强”或“弱”).
(2)N点pH>7的原因是(用化学用语表示) .
(3)下列说法正确的是(填字母).
a.M点c(HX)<c(X﹣)
b.M点c(Na+)>c(OH﹣)
c.P点c(Cl﹣)=0.05molL﹣1 .
【答案】
(1)弱
(2)X﹣+H2O?HX+OH﹣
(3)b
【解析】解:(1.)0.1molL﹣1 HCl溶液,是强酸溶液完全电离,所以溶液的PH=1;而0.1molL﹣1 HX溶液的PH>5说明是弱酸部分电离,所以答案是:弱;
(2.)N点pH>7的原因是因为两者等物质的量恰好完全反应生成强碱弱酸盐溶液水解呈碱性,所以水解反应方程式为:X﹣+H2OHX+OH﹣ , 所以答案是:X﹣+H2OHX+OH﹣;
(3.)a.M点生成等浓度的HX和NaX的混合溶液,溶液呈碱性,说明水解大于电离,所以M点c(HX)>c(X﹣),故错误;b.M点生成等浓度的HX和NaX的混合溶液,溶液呈碱性,说明水解大于电离,而水解程度微弱,所以M点c(Na+)>c(OH﹣),故正确;c.P点c(Cl﹣)= ![]() =0.067molL﹣1 , 故错误;故选:b.
=0.067molL﹣1 , 故错误;故选:b.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】R分子的质量为a g,相对质量为M,则M与a的比值等于
A.6.02×1023B.12C原子质量的十二分之一
C.0.012kg12C所含的原子数D.1mol氧气所含的微粒数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值.下列说法中,正确的是( )
A.标准状况下,22.4 L庚烷的分子数约为NA
B.密闭容器中23 g NO2与N2O4的混合气体中氮原子数为0.5NA
C.过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.4NA
D.1 L 0.1 molL﹣1的NaHCO3溶液中HCO3﹣和CO32﹣离子数之和为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海水提取溴和镁的过程如下,下列说法不正确的是( ) 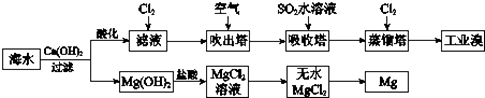
A.工业溴中含少量Cl2 , 可用NaOH溶液除去
B.工业上常利用电解熔融MgCl2冶炼金属镁
C.富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D.若提取1 mol Br2 , 至少需要标准状况下44.8 L的Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关溶液中粒子的物质的量浓度关系正确的是( )
A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl﹣)>c(OH﹣)>cCH3COO﹣)
B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3?H2O)>c(NH4+)>c(Cl﹣)>c(OH﹣)
C.0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合: ![]() c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
D.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42﹣)+c(HC2O4﹣)+c(OH﹣)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(g)与H2O(g)反应过程的能量变化如图所示,下列说法正确的是

A.该反应为吸热反应
B.CO(g)和H2O(g)的总能量大于CO2(g)和H2(g)的总能量
C.该反应的热化学方程式:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=+41 kJ/mol
CO2(g)+H2(g) ΔH=+41 kJ/mol
D.1 mol CO2(g)和1 mol H2(g)反应生成1 mol CO(g)和1 mol H2O(g)要放出41 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】列式并计算下列各小题:
(1)某温度时,测得0.01 mol/L的NaOH溶液pH为11,求该温度下水的离子积常数Kw .
(2)在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合.
①若所得混合溶液为中性,且a=12,b=2,则 Va:Vb=
②若所得混合溶液的pH=10,且a=12,b=2,则 Va:Vb= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东汉成书的《神农本草经》有“石胆化铁为铜”(石胆是硫酸铜)的记载。这一方法开创了人类文明史上湿法冶金的先河。其中涉及的化学反应类型是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2+2S2O32﹣═S4O62﹣+2I﹣
相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10﹣20 | 2.6×10﹣39 | 1.7×10﹣7 | 1.3×10﹣12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3 , 为得到纯净的CuCl22H2O晶体,加入 , 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= . 过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl22H2O晶体.
(2)在空气中直接加热CuCl22H2O晶体得不到纯的无水CuCl2 , 原因是(用化学方程式表示).由CuCl22H2O晶体得到纯的无水CuCl2的合理方法是 .
(3)某学习小组用“间接碘量法”测定含有CuCl22H2O晶体的试样(不含能与I﹣发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0molL﹣1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用作滴定指示剂,滴定终点的现象是 .
②CuCl2溶液与KI反应的离子方程式为 .
③该试样中CuCl22H2O的质量百分数为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com