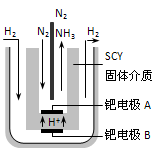
解:(1)①氨气的密度小于空气的密度,且氨气和氧气不反应,所以可以采用向下排空气法收集气体,即导气管应该“短进长出”,如图所示,
故答案为:
②氯化铵和氢氧化钙在加热条件下反应生成氯化钙、氨气和水,反应方程式为2NH
4Cl+Ca(OH)
2 
CaCl
2+2NH
3↑+2H
2O.
故答案为:2NH
4Cl+Ca(OH)
2 
CaCl
2+2NH
3↑+2H
2O.
③氨气极易溶于水,且氨气是碱性气体所以也极易溶于酸,故可以用水或酸吸收氨气.
故答案为:水(或稀盐酸、硫酸等).
(2)①氨气极易溶于水生成氨水,氨水能电离出铵根离子和氢氧根离子,导致溶液中氢氧根离子浓度大于氢离子浓度,溶液呈碱性.
故答案为:氨水显碱性(NH
3?H
2O?NH
4++OH
-).
②氨气和氯气反应生成白色烟,为氯化铵,同时还有一种相对分子质量为28的气体生成,根据反应中得失守恒和元素守恒知,另一种物质是氮气,所以反应方程式为8NH
3+3Cl
2=N
2+6NH
4Cl.
故答案为:8NH
3+3Cl
2=N
2+6NH
4Cl.
(3)氨气极易液化,气化时吸收热量,所以氨气能作制冷剂,氨气能制造吸收和化肥.
故答案为做制冷剂、制硝酸、制化肥、铵盐、纯碱等.
分析:(1)①氨气的密度小于空气的密度且和氧气不反应,所以可以采用向下排空气法收集.
②加热条件下,氯化铵和氢氧化钙反应生成氯化钙、氨气和水.
③氨气极易溶于水或酸,根据氨气的性质选取吸收剂.
(2)①氨水能电离出自由移动的氢氧根离子,导致溶液呈碱性.
②白烟是氯化铵,根据氧化还原反应中得失电子守恒和元素守恒判断另一种生成物,从而写出反应方程式.
(3)性质决定其用途,根据性质写出其相应的用途.
点评:本题考查了氨气的制取、收集和性质,难度不大,注意不能用直接加热氯化铵的方法制取氨气,因为氯化铵加热时易分解,但在导气管口,氯化氢和氨气能反应生成氯化铵固体阻塞导气管,而容易产生爆炸,所以不能用直接加热氯化铵的方法制取氨气.

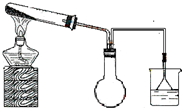 合成氨工业对化学和国防工业具有重要意义.
合成氨工业对化学和国防工业具有重要意义. 解:(1)①氨气的密度小于空气的密度,且氨气和氧气不反应,所以可以采用向下排空气法收集气体,即导气管应该“短进长出”,如图所示,
解:(1)①氨气的密度小于空气的密度,且氨气和氧气不反应,所以可以采用向下排空气法收集气体,即导气管应该“短进长出”,如图所示,
 CaCl2+2NH3↑+2H2O.
CaCl2+2NH3↑+2H2O. CaCl2+2NH3↑+2H2O.
CaCl2+2NH3↑+2H2O.

 2NH3(g);△H= -92.4 kJ/mol,
2NH3(g);△H= -92.4 kJ/mol,