

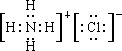 ;在常温下,向VL pH=a的氨水溶液中c(OH-)=10 a-14 mol/L,VL pH=b的盐酸溶液中c(H+)=10-b mol/L,且a+b=14,所以c(OH-)=c(H+)=10-b mol/L=10 a-14 mol/L<c(NH3.H2O),二者反应,氨水过量,溶液显碱性,pH>7,c(H+)<c(OH-) 且电荷守恒可知,则c(NH4+)>c( Cl-),故溶液中离子浓度大小顺序为c(NH4+)>c( Cl-)>c(OH-)>c(H+),故答案为:
;在常温下,向VL pH=a的氨水溶液中c(OH-)=10 a-14 mol/L,VL pH=b的盐酸溶液中c(H+)=10-b mol/L,且a+b=14,所以c(OH-)=c(H+)=10-b mol/L=10 a-14 mol/L<c(NH3.H2O),二者反应,氨水过量,溶液显碱性,pH>7,c(H+)<c(OH-) 且电荷守恒可知,则c(NH4+)>c( Cl-),故溶液中离子浓度大小顺序为c(NH4+)>c( Cl-)>c(OH-)>c(H+),故答案为: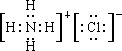 ;>;c(NH4+)>c( Cl-)>c(OH-)>c(H+).
;>;c(NH4+)>c( Cl-)>c(OH-)>c(H+).


科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等物质的量浓度溶液pH关系:pH(CH3COONa)<pH(NaHCO3)<pH(NaCN) |
| B、a mol?L-1 HCN与b mol?L-1 NaOH溶液等体积混合后溶液中c(Na+)>c(CN-),则a一定小于b |
| C、0.1mol?L-1的CH3COOH的 pH比0.1mol?L-1 HCN的pH大 |
| D、NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
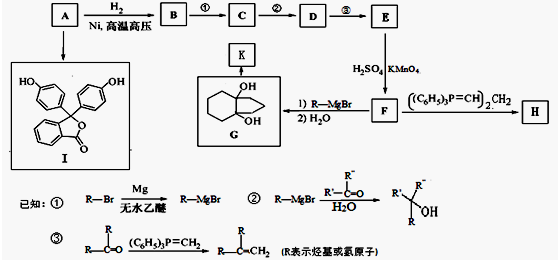
 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | B与混合气体的体积比 | 反应后气体密度(已换算为标准状况;g/L) |
| 第一次 | 1.0 | 1.35 |
| 第二次 | 1.2 | 1.25 |
| 第三次 | 2.0 | 1.04 |
| 第四次 | 2.2 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.
已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④ | B、③⑤ | C、⑦ | D、全有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子浓度:c(Na+)>c(CO32-)>c(OH-)>c(H+) |
| B、升高温度,平衡向右移动 |
| C、滴入CaCl2浓溶液,溶液的pH增大 |
| D、加入NaOH固体,溶液的pH减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com