
分析 根据饱和烃的一元衍生物燃烧通式:CxHyO+(x+$\frac{y}{4}$-$\frac{1}{2}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,结合在125℃,1.01×105Pa下完全汽化后,与其体积4.5倍的氧气混合点燃,恰好完全反应生成CO2、H2O(g),可得:x+$\frac{y}{4}$-$\frac{1}{2}$=4.5;恢复到反应前的温度、压强,测得气体的密度比反应前减小了$\frac{3}{14}$,得到,反应前后质量m不变,则$\frac{m}{5.5}$(1-$\frac{3}{14}$)=$\frac{m}{x+\frac{y}{2}}$,由方程组可得:x=3,y=8,分子式为C3H8O,可能是醇,也可能是醚,据此解答.
解答 解:饱和烃的一元衍生物燃烧通式:CxHyO+(x+$\frac{y}{4}$-$\frac{1}{2}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,结合在125℃,1.01×105Pa下完全汽化后,与其体积4.5倍的氧气混合点燃,恰好完全反应生成CO2、H2O(g),可得:x+$\frac{y}{4}$-$\frac{1}{2}$=4.5;恢复到反应前的温度、压强,测得气体的密度比反应前减小了$\frac{3}{14}$,得到,反应前后质量m不变,则$\frac{m}{5.5}$(1-$\frac{3}{14}$)=$\frac{m}{x+\frac{y}{2}}$,由方程组可得:x=3,y=8,分子式为C3H8O,属于醇有:CH3CH2CH2OH和CH3CH(OH)CH3,属于醚有:CH3CH2OHCH3,
故答案为:C3H8O;CH3CH2CH2OH、CH3CH(OH)CH3、CH3CH2OHCH3.
点评 本题考查有机物分子计算,判断分子中C、H原子数目关系,假设有机物的组成通式,再利用燃烧方程式进行计算,侧重考查学生分析计算能力,难度中等.


科目:高中化学 来源: 题型:选择题
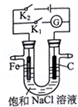
| A. | K1闭合,电流方向由铁棒经导线流向石墨棒 | |
| B. | K1闭合,向铁棒附近滴入K3[Fe(CN)6]溶液,有蓝色沉淀出现 | |
| C. | K2闭合,碳棒是阴极 | |
| D. | K2闭合,电路中通过0.2NA个电子时,两极共产生4.48 L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
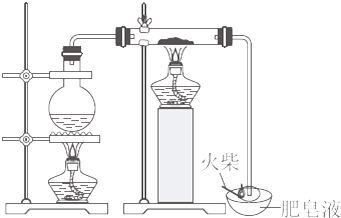
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
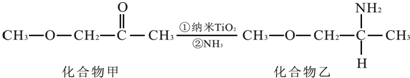
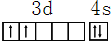 ,其原子核外共有22种运动状态不相同的电子.
,其原子核外共有22种运动状态不相同的电子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
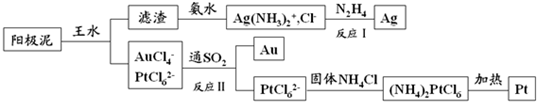
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能够完全电离的电解质称为强电解质,如硫酸、盐酸、氢氧化钠等是强电解质 | |
| B. | 1mol甲烷燃烧放出的热量为CH4的燃烧热 | |
| C. | 中和反应都有盐和水生成,有盐和水生成的反应都属于中和反应 | |
| D. | 风能是正在探索的新能源之一,它是太阳能的一种转换形式,具有不稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直链烷烃中,碳原子数越多沸点越高 | |
| B. | 碳原子数相同的烷烃,支链越多沸点越高 | |
| C. | 相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃 | |
| D. | 碳原子数相同的醇,羟基越多沸点越高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com