



 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
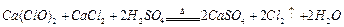 。某学习小组利用此原理设
。某学习小组利用此原理设 计如图所示装置制取氯气并探究其性质。
计如图所示装置制取氯气并探究其性质。
|

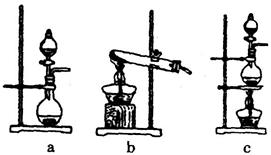 ②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填
②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填 加试剂的名称、至少填二种)方法 、
加试剂的名称、至少填二种)方法 、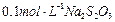 溶液:
溶液: ,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
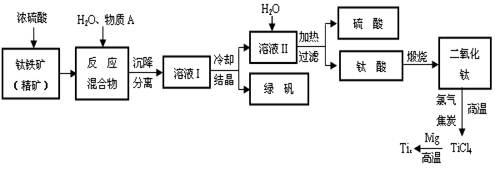
 n的值,按下列流程进行实验:
n的值,按下列流程进行实验: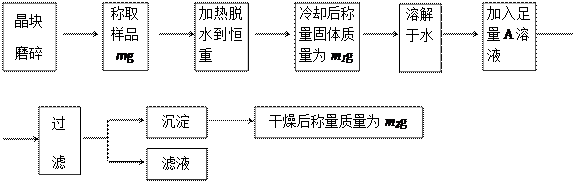
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
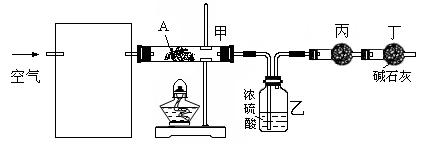
| | 甲 | 乙 | 丙 | 结论 |
| A | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| B | 盐酸 | FeS | 溴水 | 还原性:S2->Cl->Br- |
| C | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4>Cl2>Br2 |
| D | 水 | 电石 | 溴水 | 乙炔可与溴水反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在NaBr溶液中滴加几滴AgNO3溶液,产生淡黄色沉淀,再加入稀硝酸,沉淀不溶解,但溶液由无色变为黄色 |
| B.在浓HNO3中滴加紫色石蕊试液,加热最终变为无色溶液 |
| C.在NaAlO2溶液中滴加稀盐酸,无沉淀产生 |
| D.过量的Fe在氯气中燃烧,最终产物是FeCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
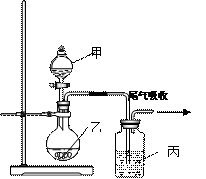
| A.采用如图所示的装置制取少量的氢氧化亚铁 |
| B.加热苯、液溴和浓硫酸的混合物制取少量的溴苯 |
| C.用素瓷片作催化剂进行石蜡油的受热分解实验 |
| D.用滴有少量硫酸铜溶液的稀硫酸跟锌粒反应快速地制氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com