
________;阴极上的反应式为________ ________.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解

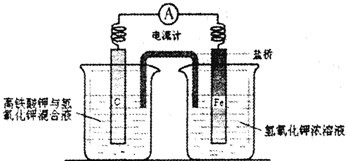
查看答案和解析>>
科目:高中化学 来源: 题型:022
向8 g某一价或二价金属的氧化物固体中加入适量的10%稀硫酸(密度为1.066 g·mL-1),使其完全溶解,已知所消耗的硫酸体积为92 mL.在所得溶液中插入铂电极进行电解.通电一定时间后,在一个电极上收集到224 mL(标准状况)氧气,在另一个电极上析出该金属1.28 g.由此可知,该金属氧化物的名称是____________;电解时阳极上的反应式为________
________;阴极上的反应式为________ ________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com