
����Ŀ��ij�о���ѧϰС����������װ��̽�������Ͱ���֮��ķ�Ӧ���������A��F�ֱ�Ϊ��������������ȡ����װ�ã�CΪ������������������İ���������Ӧ��װ�á���ش��������⣺

(1)ʵ����ͨ��������ȡ�����Ļ�ѧ����ʽΪ ________________________��
(2)ʵ�����ռ��Ʊ��õ��İ����ij��÷�����______________________��
(3)��ΪB�����߿���ѡ����ܺ��ʵ�װ���Լ���Ӧ���Լ�����______����š�
A.���θ����װ��ʯ�� B.ϴ��ƿװŨ����
C.���θ����װ������ D.���θ����װ��������
(4)װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ��д����Ӧ�Ļ�ѧ����ʽ�� __________________����1molNH3����������ת�Ƶĵ�����ĿΪ___________��
���𰸡�CaO+NH3��H2O=Ca(OH)2+NH3�� �����ſ����� ACD 3Cl2+8NH3=N2+6NH4Cl 3NA
��������
A��F�ֱ�Ϊ��������������ȡ����װ�ã�A��ΪŨ��ˮ����ʯ�ҷ�Ӧ�����ɵ��������ʢ�м�ʯ�ҵĸ���ܸ��FΪ�Ʊ�������װ�ã�EΪ��ȥHCl��װ�ã�DΪ�����ĸ���װ�ã�CΪ������������������İ���������Ӧ��װ�ã����߷���3Cl2+8NH3=N2+6NH4Cl���ɹ۲쵽�а������ɣ��Դ˽����⡣
(1)��Ũ��ˮ����ʢ��CaO����ƿ�з�����Ӧ��CaO+NH3��H2O=Ca(OH)2+NH3������ȡ�õ�������
(2)�������ܶȱȿ����£�����������ˮ������ռ������������ſ����ķ����ռ���
(3)����Ϊ�������壬���ﰱ��Ҫʹ�ü��Ը�������ﰱ�������ü�ʯ�ҡ��������ơ������Ƶȸ��ﰱ������Щ����״̬Ϊ��̬�����Ӧ��ʢ���ڸ�����У�����ACD���ϣ��ʺ���ѡ����ACD��
(4)FΪ�Ʊ�������װ�ã�Ũ����Ͷ��������ڼ��������·�Ӧ��������������ʽΪMnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O������Ũ������лӷ��ԣ������ȡ�õ��������к�������HCl��ˮ��������ͨ��װ��E��ȥ����HCl��Ȼ��ͨ��Dװ�ø������������õ��ĸ��������Cl2ͨ��Cװ���У��백��������Ӧ����װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ��˵����������NH4Cl��N2����÷�Ӧ�Ļ�ѧ����ʽΪ3Cl2+8NH3=N2+6NH4Cl�����ݷ���ʽ��֪��NԪ�صĻ��ϼ��ɷ�Ӧǰ��NH3�е�-3�۱�Ϊ��Ӧ��N2�е�0�ۣ����ϼ�������3�ۣ�ÿ1molNH3��Ӧ��ת��3mol���ӣ���ת�Ƶĵ�����ĿΪ3NA��
MnCl2+Cl2��+2H2O������Ũ������лӷ��ԣ������ȡ�õ��������к�������HCl��ˮ��������ͨ��װ��E��ȥ����HCl��Ȼ��ͨ��Dװ�ø������������õ��ĸ��������Cl2ͨ��Cװ���У��백��������Ӧ����װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ��˵����������NH4Cl��N2����÷�Ӧ�Ļ�ѧ����ʽΪ3Cl2+8NH3=N2+6NH4Cl�����ݷ���ʽ��֪��NԪ�صĻ��ϼ��ɷ�Ӧǰ��NH3�е�-3�۱�Ϊ��Ӧ��N2�е�0�ۣ����ϼ�������3�ۣ�ÿ1molNH3��Ӧ��ת��3mol���ӣ���ת�Ƶĵ�����ĿΪ3NA��


 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. ���¡���ѹ�£���һ���ɱ��ݻ��������з������·�Ӧ��A(g)��B(g)![]() C(g)
C(g)
(1)����ʼʱ����1mol A��1mol B������ƽ�������amol C����ʱA�����ʵ���Ϊ_____mol��
(2)����ʼʱ����3mol A��3mol B������ƽ�������C�����ʵ���Ϊ____mol��
(3)����ʼʱ����xmol A��2mol B��1mol C������ƽ���A��C�����ʵ����ֱ���ymol��3amol����x��___mol��y��___mol��ƽ��ʱ��B�����ʵ���________(ѡ��һ�����)��
(��)����2mol (��)����2mol (��)С��2mol (��)���ܴ��ڡ����ڻ�С��2mol
II. ��ά���¶Ȳ��䣬��һ����(1)��Ӧǰ��ʼ�����ͬ�����ݻ��̶��������з���������Ӧ��
(4)��ʼʱ����1mol A��1mol B����ƽ�������bmol C����b��(1)С���a���бȽϣ���________(ѡ��һ�����)��
(��)a<b�� (��)a>b�� (��)a��b�� (��)���ܱȽ�a��b�Ĵ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ZrO2�������մɲ��ϣ������Ӣɰ����Ҫ�ɷ�ΪZrSiO4��Ҳ�ɱ�ʾΪZrO2��SiO2����������Fe2O3��Al2O3��SiO2�����ʣ�ͨ�����·�����ȡ��
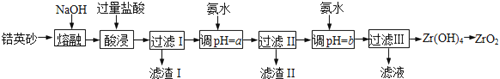
��֪����ZrO2�����ռӦ���ɿ�����ˮ��Na2ZrO3��Na2ZrO3���ᷴӦ����ZrO2+��
�����ֽ���������ʵ�������¿�ʼ��������ȫ������pH���±���
�������� | Fe3+ | Al3+ | ZrO2+ |
��ʼ����ʱpH | 1.9 | 3.3 | 6.2 |
������ȫʱpH | 3.2 | 5.2 | 8.0 |
��1������ʱZrSiO4������Ӧ�Ļ�ѧ����ʽΪ ������I�Ļ�ѧʽΪ ��
��2��Ϊʹ��ҺI���������ӳ�����ȫ�����ð�ˮ��pH=a����a�ķ�Χ�� �������Ӱ�ˮ��pH=bʱ����������Ӧ�����ӷ���ʽΪ ��
��3�������III������Һ�м���CaCO3��ĩ�����ȣ��õ��������塣�÷�Ӧ�����ӷ���ʽΪ ��
��4��Ϊ�õ�������ZrO2��Zr��OH��4��Ҫϴ�ӣ�����Zr��OH��4�Ƿ�ϴ�Ӹɾ��ķ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����仯����������������Ӧ�ù㷺���ش��������⣺
(1)��立���һ�ֻ�ѧ����,����ʽ�� NH4Fe(SO4)2��12H2O,������ˮ��,��Һ�е�����Ũ�ȴ�С��ϵΪ__________________��
(2)��֪ij��Һ�к��� CO32����SO42��������,ȡһ�����ĸ���Һ,�����еμ�BaCl2��Һ���� CO32����ʼ�� ��ʱ����Һ��c(CO32-)/c(SO42-)Ϊ_______________��(��֪ Ksp(BaSO4 )��1.0��10��10 ��Ksp(BaCO3)��2.5��10��9 )
(3)��֪��S2Cl2(l)��Cl2(g)��2SCl2(l) ��H����50.2kJ��mol��1 ������ 1molCl��Cl����1molS��S���ֱ���Ҫ���� 243kJ��268kJ ������������� 1mol S��Cl����Ҫ���յ�����Ϊ____kJ��
(4)�� NaOH ��Һ���������е� SO2,�����õ� Na2SO3 ��Һ���е��,�����Ʊ�H2SO4����ԭ������ͼ��ʾ(�缫����Ϊʯī)��
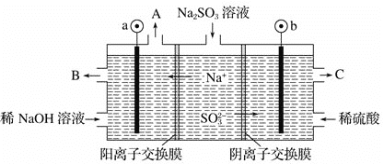
�����ĵ缫��ӦʽΪ______________________�����п�ѭ��ʹ�õ�������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ���������Ԫ�� W��M��X��Y��Z ԭ�����������������ϱ�����Ϣ�ش���������:
Ԫ�� | W | M | X | Y | Z |
�ṹ������ | ��ۺ��� ��������̬ �⻯���ܷ� �����Ϸ�Ӧ | �⻯���ˮ ��Һ�ܿ�ʴ ���� | ��ɫ��Ӧ�� ��ʻ�ɫ | ͬ��������Ԫ ���γɵļ� �����У������� �뾶��С | ��������� ����۴� ����Ϊ 6 |
(1)MԪ�������ڱ��е�λ��Ϊ_____��
(2)M��X��ZԪ������Ӧ�����Ӱ뾶�ɴ�С��˳��Ϊ_____________________(�����ӷ��ű�ʾ)��
(3)W��ۺ�����������̬�⻯������Ϸ�Ӧ���ɵ������к��еĻ�ѧ������Ϊ___________________________________��
(4)���п���Ϊ�Ƚ�M��Z�ķǽ�����ǿ����������_________(�����)��
A.������H2��Ӧ�����׳̶�
B.�⻯����ȶ���
C.����������ˮ��������ǿ��
D.��M�ĵ���ͨ��Z��������Һ�۲��Ƿ���Z�ݳ�
(5)W���γɶ����⻯�����һ���⻯�����Ϊ���ȼ�ϣ���������W����Ԫ�ص�������Ϊ7:1��д�����⻯��ĵ���ʽ______�����⻯��� O2 �ڼ��������¿��γ�ȼ�ϵ�أ��������������ʣ�д���为���ĵ缫��Ӧʽ___________.
(6)YԪ�غ�WԪ���γɵĻ�����YWһ�����������ϣ���������ռ���Һ��Ӧ����ʹʪ��ĺ�ɫʯ����ֽ���������壬д���йصĻ�ѧ����ʽ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������½�����A��B���ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g) ![]() 2C(g)+2D(g)����Ӧ���е�10sĩ���ﵽƽ�⣬���A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
2C(g)+2D(g)����Ӧ���е�10sĩ���ﵽƽ�⣬���A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
(1)��C��ʾ10s������Ӧ�Ļ�ѧ��Ӧ����Ϊ___________��
(2)��ӦǰA�����ʵ���Ũ����___________��
(3)ƽ��ʱA��ת����Ϊ___________��
(4)��˵���÷�Ӧ�ﵽƽ��״̬����______________��
A.����3molAͬʱ����2molC B.��Ӧ��ϵ�и����ʵİٷֺ�������
C.�������ƽ����Է����������� D.2V��(A)=3V��(C)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. ��������Һ�м����������������Һ��SO42-��Ba2�� ![]() BaSO4��
BaSO4��
B. ��CH3COOH�м�������������������Һ�� CH3COOH��OH�� ![]() CH3COO����H2O
CH3COO����H2O
C. �������������м���������ϡ���Fe(OH)2 ��2H��![]() Fe2����2H2O
Fe2����2H2O
D. ��̼�������Һ�м�������������������Һ��NH4+�� OH�� ![]() NH3��H2O
NH3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�������Һ�д����������
A.H+��Ca2+��Cl-��CO32-B.I-��ClO-��K+��H+
C.Na+��Fe3+��SO42-��OH- D.Na+��Cu2+��Cl-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ�Ⱦ�Ϊ0.1mol/L�����ΪV0��HX��HY��Һ���ֱ��ˮϡ�������V��pH��lg(V/ V0)�ı仯��ϵ��ͼ��ʾ������������ȷ����( )

A. HX��HY�������ᣬ��HX�����Ա�HY����
B. ��ͬ�¶��£����볣��K(HX):a>b
C. �����£���ˮ�������c(H+)��c(OH-):a<b
D. lg(V/ V0)=3����ͬʱ��������Һ����[c(X-)/c(Y-)]��С
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com