
【题目】
铜矿( CuFeS2)是炼铜的最主要矿物。火法冶炼黄钢矿的过程中,其中一步反应是:2Cu2O+Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+价电子的电子排布图为___________,Cu2O与Cu2S比较,熔点较高的是___________,原因为______________________。
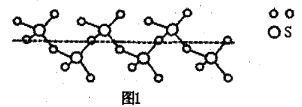
(2)SO2与SO3的键角相比,键角更小的是___________。某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图1所示。此固态物质中S原子的杂化轨道类型是___________;该物质的化学式为___________。
(3)离子化合物CaC2的晶体结构如图2所示。写出该物质的电子式___________。从钙离子看该晶体属于___________堆积,一个晶胞含有的π键平均有___________个。

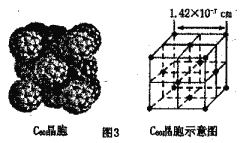
(4)根据图3可知,与每个C60分子距离最近且相等的C60分子有___________个,其距离为___________cm(列出计算式即可)。
【答案】![]() Cu2O 两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高 SO2 sp3 SO3或(SO3)n
Cu2O 两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高 SO2 sp3 SO3或(SO3)n ![]() 面心立方 8 12
面心立方 8 12 ![]()
【解析】
(1)Cu位于第四周期IB族,Cu+的价电子为第三层的d能级,根据泡利原理和洪特规则,书写价电子轨道式;Cu2O和Cu2S都属于离子晶体,晶格能越大,晶体熔沸点越高,据此分析作答;
(2)孤电子对之间的斥力>孤电子对-成键电子对之间的斥力>成键电子对之间斥力,据此分析键角大小;利用均摊法求出图1中的化学式组成,再请根据杂化轨道类型判断其杂化方式;
(3)碳化钙中存在离子键与非极性共价键,据此写出其电子式;结合金属原子常见堆积模型作答;再根据均摊法计算所含π键数目。
(1)Cu位于第四周期IB族,Cu+的价电子为第三层的d能级,根据泡利原理和洪特规则,Cu+价电子轨道式为![]() ;Cu2O和Cu2S都属于离子晶体,晶格能越大,晶体熔沸点越高,晶格能与半径、所带电荷数有关,半径越小、所带电荷数越多,晶格能越大,Cu2O和Cu2S所带电荷数相同,S2-的半径大于O2-的半径,因此Cu2S的沸点低于Cu2O;
;Cu2O和Cu2S都属于离子晶体,晶格能越大,晶体熔沸点越高,晶格能与半径、所带电荷数有关,半径越小、所带电荷数越多,晶格能越大,Cu2O和Cu2S所带电荷数相同,S2-的半径大于O2-的半径,因此Cu2S的沸点低于Cu2O;
故答案为![]() ;Cu2O;两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高;
;Cu2O;两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高;
(2)SO2含有的孤电子对为(6-2×2)/2=1,SO3中含有孤电子对为(6-2×3)/2=0,孤电子对之间的斥力>孤电子对-成键电子对之间的斥力>成键电子对之间斥力,因此SO3键角大于SO2键角;根据图1可知,该固体结构的基本单元中含S原子数目为1个,O原子数目为![]() =3个,所以其化学式为SO3或(SO3)n,又因为中心S有4个σ键,无孤电子对,价层电子对数为4,杂化轨道数等于价层电子对数,即杂化类型为sp3;
=3个,所以其化学式为SO3或(SO3)n,又因为中心S有4个σ键,无孤电子对,价层电子对数为4,杂化轨道数等于价层电子对数,即杂化类型为sp3;
故答案为SO2;sp3;SO3或(SO3)n;
(3)根据图2,CaC2的电子式为:![]() ;根据晶胞的结构,Ca2+位于顶点和面心,因此属于面心立方堆积;C22-位于棱上和体心,属于晶胞的C22-的个数为12×1/4+1=4,根据CaC2的电子式,两个碳原子之间有3对电子对,即1个C22-有2个π键,即1个晶胞中有2×4=8个π键;
;根据晶胞的结构,Ca2+位于顶点和面心,因此属于面心立方堆积;C22-位于棱上和体心,属于晶胞的C22-的个数为12×1/4+1=4,根据CaC2的电子式,两个碳原子之间有3对电子对,即1个C22-有2个π键,即1个晶胞中有2×4=8个π键;
故答案:![]() ;面心立方; 8。
;面心立方; 8。
(4)根据图3,与每个C60分子距离最近且相等的C60分子有12个,其距离等于边长的![]() ,所以其距离 =
,所以其距离 = ![]() ,
,
故答案为12;![]() 。
。


科目:高中化学 来源: 题型:
【题目】根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是( )
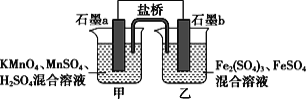
A.石墨b是原电池的负极,发生氧化反应
B.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol
C.甲烧杯中的电极反应式:MnO4-+5e-+8H+=Mn2++4H2O
D.电池工作时,盐桥中的K+向甲烧杯中移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个体积为2L的密闭容器中,高温下发生反应:C(s)+H2O(g)![]() CO(g)+H2(g),其中,H2O、CO的物质的量随时间的变化曲线如下图所示。
CO(g)+H2(g),其中,H2O、CO的物质的量随时间的变化曲线如下图所示。

(1)写出上述反应的平衡常数表达式K=______。
(2)计算第1min内v(H2O)=_______。
(3)反应处于平衡状态的时间段是_______。
(4)若反应进行至2min时,改变了温度,使曲线发生了如下图所示的变化,则温度是____,(填“升高、降低、不变”),正反应是_____(填“吸热、放热”)反应。
(5)反应至5min时,若也只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是下述中的____(填写编号)。
①增加了CO; ②增加了水蒸气; ③加了催化剂; ④扩大了容器体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
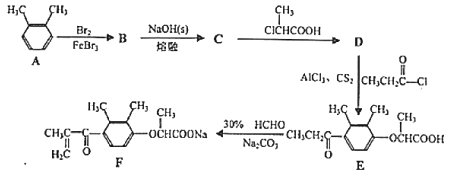
【题目】化合物F是一种药物合成的中间体,F的一种合成路线如下:
已知:
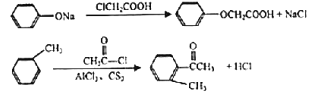
回答下列问题:
(1)![]() 的名称为____。
的名称为____。
(2)D中含氧官能团的名称为____。
(3)B→C的反应方程式为____。
(4)D→E的反应类型为____。
(5)C的同分异构体有多种,其中苯环上连有—ONa、2个—CH3的同分异构体还有____种,写出核磁共振氢谱为3组峰,峰面积之比为6:2:1的同分异构体的结构简式____。
(6)依他尼酸钠( )是一种高效利尿药物,参考以上合成路线中的相关信息,设计以
)是一种高效利尿药物,参考以上合成路线中的相关信息,设计以![]() 为原料(其他原料自选)合成依他尼酸钠的合成路线。________________
为原料(其他原料自选)合成依他尼酸钠的合成路线。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:

已知:“反应Ⅱ”的离子方程式为Cu2++CuS+4C1-==2[CuCl2]-+S
回答下列问题:
(1)铁红的化学式为__________________;
(2)“反应Ⅱ”的还原剂是_______________(填化学式);
(3)“反应III”的离子方程式为____________________________________;
(4)辉铜矿的主要成分是Cu2S,可由黄铜矿(主要成分CuFeS2)通过电化学反应转变而成,有关转化如下如图 所示。转化时正极的电极反应式为___________________。
(5)从辉铜矿中浸取铜元素,可用FeCl3作浸取剂。
①反应Cu2S+4FeCl32CuCl2+4FeCl2+S,每生成1mol CuCl2,反应中转移电子的数目为______;浸取时,在有氧环境下可维持Fe3+较高浓度。有关反应的离子方程式是__________。
②浸取过程中加入洗涤剂溶解硫时,铜元素的浸取率的变化如图,其原因是_______________。


(6)CuCl悬浊液中加入Na2S,发生的反应为2CuCl(s)+S2-(aq)![]() Cu2S(s)+2Cl-(aq),该反应的平衡常数K =__________________[已知Ksp(CuCl)=1.2×10-6, Ksp(Cu2S)=2.5×10-43]。
Cu2S(s)+2Cl-(aq),该反应的平衡常数K =__________________[已知Ksp(CuCl)=1.2×10-6, Ksp(Cu2S)=2.5×10-43]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应H2(g)+Br2(g)![]() 2HBr(g);ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g);ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
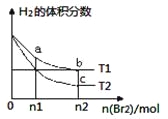
A. 若b、c点的平衡常数分别为K1、K2,则K1>K2
B. a、b两点的反应速率:b>a
C. 为了提高Br2(g)的转化率,可采取增加Br2(g)通入量的方法
D. 若平衡后保持温度不变,压缩容器体积平衡一定不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下进行如下反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度B.加催化剂同时增大压强
C.升高温度同时充入N2D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在国庆70周年庆典上,空中飞过的歼击机编队让我们热血沸腾,其中有中国自主研制的最先进的歼20隐形超音速飞机。当超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层,,或许通过测定局部的臭氧浓度变化可使飞机不再“隐形”。因此科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H<0。请回答下列问题:
2CO2(g)+N2(g) △H<0。请回答下列问题:
(1)该反应的平衡常数表达式为___________________________。
(2)假设在闭容器发生上述反应,达到平衡后采取下列选项的措施既能加快反应速率又能提高NO转化率的是_____________。
A.选用更有效的催化剂同时增加CO的量 B.升高反应体系的温度
C.及时加入碱石灰 D.缩小容器的体积
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学将等物质的量的NO和CO充入容积为2L的恒容密闭容器中,设计了三组实验,部分实验数据已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度/mol·L-1 | NO平衡浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
Ⅰ | 280 | 0.3 | 0.1 | 82 |
Ⅱ | T1 | c1 | c2 | 124 |
Ⅲ | 350 | c3 | c4 | 124 |
①在上述表格的实验条件数据中,T1=____________,c3=_____________。
②平衡时若保持温度T1℃不变,再向容器中充入CO和CO2各0.2mol,则平衡将_________移动(填“向左”“向右”或“不”)

③在给出的坐标图中,画出了上表中的I、Ⅱ、Ⅲ实验条件下建立平衡过程中,混合气体里NO浓度随时间变化的趋势曲线图,请说出B曲线对应的实验编号__________(填Ⅱ、Ⅲ)。

(4)在恒温恒容的密闭容器中通入n(NO):n(CO)=1:3的混合气体,发生上述反应,下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①I2(g)+H2(g)![]() 2HI(g) ΔH1=-9.48 kJ/mol
2HI(g) ΔH1=-9.48 kJ/mol
②I2(s)+H2(g)![]() 2HI(g) ΔH2=+26.48 kJ/mol
2HI(g) ΔH2=+26.48 kJ/mol
下列判断正确的是( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.I2(g)=I2(s) ΔH=-17.00 kJ/mol
C.固态碘的稳定性比气态碘的稳定性高
D.1 mol固态碘和1 mol气态碘分别与氢气完全反应,前者断裂的I—I键更多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com