
【题目】已知H2O2的结构如下图:

H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:
(1)写出H2O2分子的电子式和结构式。___________
(2)写出分子内的键型。__________
(3)估计它难溶于CS2,简要说明原因。_________
(4)指出氧元素的化合价,简要说明原因。____________
【答案】![]()
![]() 分子内既有极性键,又有非极性键 因H2O2为极性分子,而CS2为非极性溶剂,根据相似相溶规则,H2O2难溶于CS2中 氧为-1价,因O—O键为非极性键,而O—H键为极性键,共用电子对偏向氧,故氧为-1价。
分子内既有极性键,又有非极性键 因H2O2为极性分子,而CS2为非极性溶剂,根据相似相溶规则,H2O2难溶于CS2中 氧为-1价,因O—O键为非极性键,而O—H键为极性键,共用电子对偏向氧,故氧为-1价。
【解析】
根据双氧水的结构和性质,双氧水中化学键的类型分析解答。
(1)双氧水是一种含有氧氧共价键和氧氢共价键的极性分子,电子式为:![]() ,结构式为:H—O—O—H;
,结构式为:H—O—O—H;
(2) 双氧水中氢与氧形成的是极性键,氧与氧形成的是非极性键;
(3) 相似相溶原理是指由于极性分子间的电性作用,使得极性分子组成的溶质易溶于极性分子组成的溶剂,难溶于非极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂,难溶于极性分子组成的溶剂,H2O2是极性分子,CS2是非极性分子,依据相似相溶的原理可知,H2O2难溶于CS2;
(4) 在双氧水中,O-O键非极性键,而O-H键为极性键,氧原子得电子的能力强,共用电子对偏向氧,故氧为-1价。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡状态标志的是①单位时间内生成a mol A,同时生成3a mol B;②C生成的速率与C分解的速率相等; ③A、B、C的浓度不再变化;④A、B、C的压强不再变化;⑤混合气体的总压强不再变化;⑥A、B、C的分子数之比为1∶3∶2⑦单位时间内消耗a mol A,同时生成3a mol B;⑧混合气体的物质的量不再变化;
2C(g)达到平衡状态标志的是①单位时间内生成a mol A,同时生成3a mol B;②C生成的速率与C分解的速率相等; ③A、B、C的浓度不再变化;④A、B、C的压强不再变化;⑤混合气体的总压强不再变化;⑥A、B、C的分子数之比为1∶3∶2⑦单位时间内消耗a mol A,同时生成3a mol B;⑧混合气体的物质的量不再变化;
A. ②⑧ B. ①⑥ C. ②④ D. ③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)xC(g),有图 I(T表示温度,P 表示压强,C%表示 C 的体积分数)所示的反应曲线,试判断对图 II 的说法中正确的是

A. 若 P3>P4,则 y 轴表示 B 的百分含量
B. 若 P3>P4,则 y 轴表示混合气体的平均摩尔质量
C. 若 P3<P4,则 y 轴表示 B 的体积分数
D. 若 P3<P4,则 y 轴表示混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铜矿(主要成分是CuFeS2)为原料炼铜的方法为火法炼铜和湿法炼铜两种。
(1)火法炼铜时产生大量SO2,根据原电池原理,稀硫酸作电解质溶液,使用惰性电极,一极通入SO2,另一极通入O2,治理SO2污染,负极反应的离子方程式为___________________________。
(2)火法炼铜的过程中,电解出铜制备精铜时产生的废电解液中含有较多Ni2+和Pb2+,从废电解液中除去Pb2+的方法是往其中通入H2S至饱和,使Pb2+转化为硫化物沉淀(已知饱和H2S溶液中c(H2S)为0.1mol/L,![]() ≈10-20;Ksp(NiS)≈10-11)。若废电解液的pH=5,为保证不生成沉淀,Ni2+浓度应控制在_________mol/L以下。
≈10-20;Ksp(NiS)≈10-11)。若废电解液的pH=5,为保证不生成沉淀,Ni2+浓度应控制在_________mol/L以下。
(3)近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐。某工厂运用该原理生产铜和绿矾(FeSO4·7H2O)的工艺如图:

①写出反应的化学反应方程式:___________________________;如果对该反应进行高温加热,发现化学反应速率降低乃至反应停止,请简述理由:___________________________。
②固体A的成分为___________________________。
③欲从滤液中获得绿矾晶体,分离操作I因为_________、_________、过滤。
④写出反应湿法炼铜的化学反应方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸普鲁卡因 (  ) 是一种良好的局部麻醉药, 具有毒性小, 无成瘾性等特点。其合成路线如下图所示:
) 是一种良好的局部麻醉药, 具有毒性小, 无成瘾性等特点。其合成路线如下图所示:

回答下列问题:
(1) 3molA可以合成1molB, 且B是平面正六边形结构, 则B的结构简式为_________。
(2) 有机物C的名称为____________, B→C的反应类型为_____________。
(3) 反应C→D的化学方程式为________________________________________。
(4) F和E发生酯化反应生成G, 则F的结构简式为___________________。
(5) H的分子式为____。
(6) 分子式为C9H12且是C的同系物的同分异构体共有__________种。
(7) 请结合上述流程信息, 设计由苯、 乙炔为原料合成 的路线_______________ 。(其他无机试剂任选)
的路线_______________ 。(其他无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________。人一旦吸入b气体后,就易引起中毒,是因为__________而中毒。
(3)c是双核单质,写出其电子式____________。c分子中所含共价键的类型为_______(填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________。
(4)d是四核化合物,其结构式为______________;d分子内所含共价键有________个σ键,________个π键;σ键与π键的强度大小关系为σ___π(填“>”、“<”或“=”),原因是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种免疫调节剂,其结构简式如图所示,关于该物质的说法不正确的是
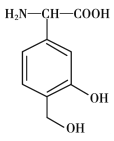
A. 属于芳香族化合物,分子式为C9H11O4N
B. 可以发生的反应类型有:加成反应、取代反应、氧化反应、聚合反应
C. 分子中所有碳原子有可能在同一平面上
D. 1mol该调节剂最多可以与3 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室现有一包NaCl、FeCl3、Al2(SO4)3组成的粉末,某课外小组同学为测定其中NaCl的含量,取13.69 g样品进行如下实验(所加试剂均为过量)。

请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是______(填序号)。
(2)生成沉淀C的离子方程式是_________________________________。
(3)根据上述实验,判断下列说法正确的是______(填字母)。
a.溶液D是无色的碱性溶液
b.溶液D中至少含有5种离子
c.向溶液D中加入过量稀硫酸,产生白色沉淀
d.仅用硝酸银一种试剂不能检验溶液D中的氯离子
(4)样品中NaCl的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究性学习实验小组做了如下实验:
实验一:利用H2C2O4 溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
实验序号 | 试验温度/K | 溶液颜色褪至无色时所需时间/s | |||||
KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 5 | 0.1 | 3 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 5 | t1 |
(1)通过实验A、B,可探究出_____________ (填外部因素)的改变对反应速率的影响,其中V1=__________,T1=__________;通过实验__________可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由此实验可以得出的结论是_______________;利用实验B 中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4span>)= __________。
实验二:探究酸的强弱对酸与镁条反应速率的影响。
实验步骤:


(a)检查装置的气密性后,添加药品;
(b)反应开始后,每隔1min记录一次生成H2的体积;
(c)将所记录的数据转化为曲线图(上图乙)。
(3)根据反应的图像(图乙)分析:0-lmin盐酸与镁反应比1-2min反应快的原因:_____________。
(4)对照实验:用20mL水代替酸进行实验。
实验现象:当水滴入锥形瓶中,注射器的活塞_________(填“会”或“不会”)向右移动。
问题分析:针对上述现象,上图中气体发生装置是否合理:_______(填“合理”或“不合理”)若合理,则忽略下问;若不合理,请改进上述装置使其变成合理的装置图:_____________ (用必要的文字或装置图进行回答)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com