
【题目】在 A+2B3C+4D 反应中,表示该反应速率最快的是( )
A.v(A)=0.3 mol/(Ls)
B.v(B)=0.5 mol/(Ls)
C.v(C)=0.8 mol/(Ls)
D.v(D)=1 mol/(Lmin)
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】设NA 为阿伏加德罗常数的值.下列说法正确的是( )
A.标准状况下,2.24 Cl2完全反应生成FeCl3或CuCl2 , 转移的电子数都为0.2NA
B.18g D2O中含有的电子数为10 NA
C.pH=12的氨水中含有NH4+的数目为0.01 NA
D.28g 由乙烯和CO组成的混合物中含有的原子总数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
a、2NO(g)+Cl2(g)2ClNO(g)△H1<0 其平衡常数为K1
b、2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)△H2<0 其平衡常数为K2
(1)4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)△H3的平衡常数K=(用K1、K2表示).△H3=(用△H1、△H2表示).
(2)为研究不同条件对反应a的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2 , 10min时反应a达到平衡.测得10min内V(ClNO)=7.5×10﹣3molL﹣1min﹣1 , 则平衡后n(Cl2)=mol,NO的转化率α1= . 其它条件保持不变,反应(1)在恒压条件下进行,平衡时NO的转化率为α2 , α1α2(填“>”“<”或“=”),平衡常数K1(填“增大”“减小”或“不变”).若要使K1减小,可采用的措施是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图1装置进行实验,试回答下列问题. 
(1)若开始时开关K与a连接,则B极的电极反应式为 .
(2)若开始时开关K与b连接,总反应的离子方程式为有关上述(2)实验,下列说法正确的是(填序号) .
①溶液中Na+向A极移动
②若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾.
①该电解槽的阳极反应式为 . 此时通过阳离子交换膜的离子数(填“大于”、“小于”或“等于”)通过阴离子交换膜的离子数.
②若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为 2CH3OH+3O2+4KOH═2K2CO3+6H2O.下列说法正确的 是( ) 
A.若将乙池电解液换成 AgNO3 溶液,则可以实现在石墨棒上镀银
B.甲池通入 CH3OH 的电极反应式为 CH3OH+6e﹣+2H2O═CO32﹣+8H+
C.反应一段时间后,向乙池中加入一定量 Cu(OH)2 固体,能使 CuSO4溶液恢复到 原浓度
D.甲池中消耗 224mL(标准状况下)O2 , 此时丙池中理论上产生 1.16g 固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列 关于该电池的叙述错误的是( ) 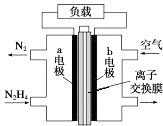
A.b 极发生还原反应
B.a 极的反应式为 N2H4﹣4e﹣═N2↑+4H+
C.放电时,电流从 b 极经过负载流向 a 极
D.其中的离子交换膜需选用阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为0.1molL﹣1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg ![]() 随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( ) 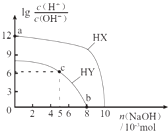
A.HX的酸性弱于HY
B.a点由水电离出的c(H+)=10﹣12 molL﹣1
C.c点溶液中:c(Y﹣)>c(HY)
D.b点时酸碱恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀Na2SO4溶液混合,装在半透膜中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是
A. 加入BaCl2溶液产生白色沉淀 B. 加入碘水不变蓝
C. 加入BaCl溶液没有白色沉淀产生 D. 加入碘水变蓝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com