
 ����10��Ԫ�ص����ʡ��������±����У����Ǿ�Ϊ������Ԫ�أ�
����10��Ԫ�ص����ʡ��������±����У����Ǿ�Ϊ������Ԫ�أ�| A | B | C | D | E | F | G | H | I | J | |
| ԭ�Ӱ뾶��10-10m�� | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| ������ ���ϼ� | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
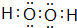 �����ɸ����ʵĻ�ѧ�������м��Լ��ͷǼ��Լ�������A��B�γɻ�������γɹ��̱�ʾʽ��
�����ɸ����ʵĻ�ѧ�������м��Լ��ͷǼ��Լ�������A��B�γɻ�������γɹ��̱�ʾʽ�� _��
_��
���� ��1��������Ԫ���У�A��I����-2�ۣ�����VIA�壬��I��+6�ۣ�ԭ�Ӱ뾶Ҳ�ϴ�AΪ����IΪ��D��G����+5��-3�ۣ���D��ԭ�Ӱ뾶�ϴ�DΪ�ס�GΪ����E��+7��-1�ۣ���EΪCl��C��F��J�������+1������IA�壬ԭ�Ӱ뾶F��C��J����FΪNa��CΪLi��JΪ�⣻B��+2�ۣ�H��+3�ۣ��ֱ��ڢ�A�塢��A�壬��ԭ�Ӱ뾶B���ף�H��Cl����BΪMg��HΪ��
��2��������ǿ�Ļ�������Ǹ����
������J2A2ΪH2O2����ԭ��֮���γ�1�Թ��õ��Ӷԣ���ԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ�
A��B�γɻ�����ΪMgO����þ�����������ӹ��ɣ�
��3����ԭ��Fe2+��Br-��ͨ�������ȷ�����Ӧ2Fe2++Cl2�T2Fe3++2Cl-��Fe2+��Ӧ��ϣ�ʣ��������ٷ�����Ӧ2Br-+Cl2�TBr2+2Cl-���������ӷ���ʽ���㱻����Br-�����ʵ�����������д�ܷ�Ӧ���ӷ���ʽ��
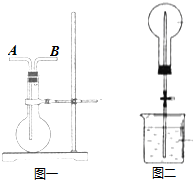
��4��G���⻯��ΪNH3���ܶȱȿ���С����ȡ�����ſ������ռ���
����ë������ƿ���ȣ�NH3�������ͣ��ϳ����������ڵĿ�����ˮ��NH3��ˮ�Ӵ���
ƿ��������ܶ�����ͬ�����������ܶȵ�10.5������ƽ����Է�������Ϊ21������ƿ�ڰ�������������֮�ȣ�Һ���������Ϊ�����ڰ��������
��5���������������������ǿ�����ԣ���������������Ϊ�����ӣ���������ԭΪNO��
��6��SO2��Na2O2��Ӧ������CO2��Na2O2�ķ�Ӧ����Ӧ����Na2SO3��O2��
����Na2O2�ὫSO32-����ΪSO42-�������ϡ����Ҳ�ܽ�BaSO3����ΪBaSO4��
��� �⣺��1��������Ԫ���У�A��I����-2�ۣ�����VIA�壬��I��+6�ۣ�ԭ�Ӱ뾶Ҳ�ϴ�AΪ����IΪ��D��G����+5��-3�ۣ���D��ԭ�Ӱ뾶�ϴ�DΪ�ס�GΪ����E��+7��-1�ۣ���EΪCl��C��F��J�������+1������IA�壬ԭ�Ӱ뾶F��C��J����FΪNa��CΪLi��JΪ�⣻B��+2�ۣ�H��+3�ۣ��ֱ��ڢ�A�塢��A�壬��ԭ�Ӱ뾶B���ף�H��Cl����BΪMg��HΪ��
�ʴ�Ϊ���ף�B��
��2��������ǿ�Ļ��������HClO4��
������J2A2ΪH2O2������ʽΪ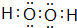 �����м��Լ��ͷǼ��Լ���
�����м��Լ��ͷǼ��Լ���
A��B�γɻ�����ΪMgO����þ�����������ӹ��ɣ��õ���ʽ��ʾ�γɹ��̣� ��
��
�ʴ�Ϊ��HClO4��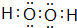 �����Լ��ͷǼ��Լ���
�����Լ��ͷǼ��Լ��� ��
��
��3��3.36L�������ʵ���Ϊ$\frac{3.36L}{22.4L/mol}$=0.15mol��FeBr2���ʵ���Ϊ0.1L��2mol/L=0.2mol��
��ԭ��Fe2+��Br-��ͨ�������ȷ�����Ӧ2Fe2++Cl2�T2Fe3++2Cl-��Fe2+��ȫ��Ӧ��������Ϊ0.2mol��$\frac{1}{2}$=0.1mol��ʣ������Ϊ0.15mol-0.1mol=0.05mol��ʣ��������ٷ�����Ӧ2Br-+Cl2�TBr2+2Cl-��0.05mol������Ӧ����Br-Ϊ0.05mol��2=0.1mol��Br-��ʣ�࣬�ʷ�Ӧ��������Fe2+��Br-�����ʵ���֮��Ϊ0.15mol��0.2mol��0.1mol=3��4��2�����ܷ�Ӧ���ӷ���ʽ��3Cl2+4Fe2++2Br-=6Cl-+4Fe3++Br2 ��
�ʴ�Ϊ��3Cl2+4Fe2++2Br-=6Cl-+4Fe3++Br2 ��
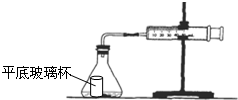
��4��G���⻯��ΪNH3���ܶȱȿ���С����ȡ�����ſ������ռ�������Ӧ��ͼһ�� B�ڽ�����ƿ��
����ë������ƿ���ȣ�NH3�������ͣ��ϳ����������ڵĿ�����ˮ��NH3��ˮ�Ӵ�����������Ȫ��
ƿ��������ܶ�����ͬ�����������ܶȵ�10.5������ƽ����Է�������Ϊ10.5��2=21���谱���������Ϊx����17x+29��1-x��=21�����x=$\frac{2}{3}$��ʵ�����Һ�彫�����������ݻ���$\frac{2}{3}$��
�ʴ�Ϊ��B������ë������ƿ���ȣ�NH3�������ͣ��ϳ����������ڵĿ�����ˮ��NH3��ˮ�Ӵ�����������Ȫ��$\frac{2}{3}$��
��5���������������������ǿ�����ԣ���������������Ϊ�����ӣ���������ԭΪNO����Ӧ���ӷ���ʽΪ��3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
�ʴ�Ϊ��3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
��6��SO2��Na2O2��Ӧ������CO2��Na2O2�ķ�Ӧ����Ӧ����Na2SO3��O2���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2SO2=2Na2SO3+O2��
����Ӧ��Ĺ����л�������Na2O2��������ˮ������Na2O2�ὫSO32-����ΪSO42-����ʹNa2O2����ȫ��Ӧ�������ϡ����Ҳ�ܽ�BaSO3����ΪBaSO4���ʸ÷�����������
�ʴ�Ϊ��2Na2O2+2SO2=2Na2SO3+O2��������������Ӧ��Ĺ����л�������Na2O2��������ˮ������Na2O2�ὫSO32-����ΪSO42-����ʹNa2O2����ȫ��Ӧ�������ϡ����Ҳ�ܽ�BaSO3����ΪBaSO4��
���� ���������ۺ�����Ŀ���漰�ṹ����λ�ù�ϵӦ�á�����ʽ�����ӷ���ʽ��д����ѧʵ�顢��ѧ����ȣ�ע�����ԭ�Ӱ뾶�뻯�ϼ��ƶ�Ԫ�أ��Ƕ�ѧ���ۺ������Ŀ��飮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��֬ | B�� | ���� | C�� | ������ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.5mol����Fe����������������ȫȼ�գ�ʧȥ4NA������ | |
| B�� | ��25g��������Ϊ60%������ˮ��Һ�У�������ԭ����ΪNA | |
| C�� | 7.8��gNa2S��Na2O2���Ļ�����У����е�������������0.15NA | |
| D�� | ��5��107Pa��500��C������ý�����£�1molN2��3molH2�����ɰ���������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
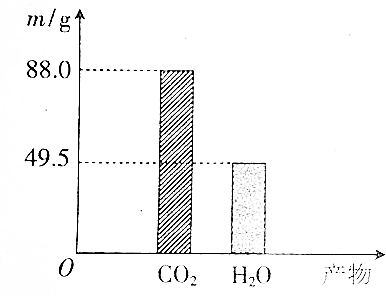
 ������̼��Ʒ�Ӧ����CO2��������ͼ��ͨ������һ��ʱ���ڲ���CO2�����������ɲⶨ�÷�Ӧ�����ʣ�������29.5�森�����Ҫ����գ�
������̼��Ʒ�Ӧ����CO2��������ͼ��ͨ������һ��ʱ���ڲ���CO2�����������ɲⶨ�÷�Ӧ�����ʣ�������29.5�森�����Ҫ����գ�| ʱ��/s | 10 | 20 | 30 | 40 | 50 | 60 |
| �������/mL | 4 | 14 | 25 | 38 | 47 | 55 |
| ��Ӧ����/mL•s-1 | 0.4 | 1.0 | 1.1 | 1.3 | 0.9 | 0.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na2O2+2H2O�T4NaOH+O2�� | B�� | Mg3Cl2+2NaOH�TMg��OH��2��+2NaCl | ||
| C�� | 2NaOH+Cl2�TNaOCl+H2O | D�� | NH4Cl+NaO�TNaCl+NH3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
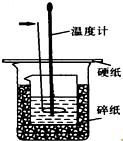 50ml0.50mol•L-1������50mL0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺
50ml0.50mol•L-1������50mL0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com