
【题目】100℃时,在不同金属离子存在下,过氧化氢经过24h的分解率如下表所示:
离子 | 加入量(mg·L-1) | 分解率/% | 离子 | 加入量(mg·L-1) | 分解率/% |
无 |
| 2 | Fe2+ | 1.0 | 15 |
Al3+ | 10 | 2 | Cu2+ | 0.1 | 86 |
Zn2+ | 10 | 10 | Cr3+ | 0.1 | 96 |
下列有关说法正确的是
A.能使过氧化氢分解反应活化能降低最多的离子是Al3+
B.催化剂可以使平衡移动,提高过氧化氢的分解率
C.若向过氧化氢中加入水,过氧化氢的分解速率加快
D.用等量H2O2制O2时,与自身分解相比,加入足量酸性KMnO4溶液可得到更多O2
科目:高中化学 来源: 题型:
【题目】TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元素组成,M=240g/mol。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。主要过程为在足量氧气流中将4.80 g TMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热装置等已略去,其他用品可自选)。
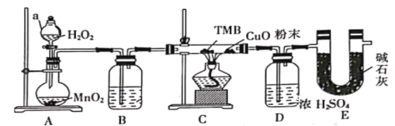
(1)写出仪器a的名称__________,A中的化学反应方程式:___________;
(2)B中试剂是___________,作用是________________ ;
(3)装置C中CuO粉末的作用为________________。
(4)理想状态下,将4.80 gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60 g,E增加14.08 g,则TMB的分子式为____________。
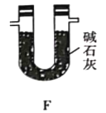
(5)有同学认为,用该实验装置测得的TMB分子式不准确,应在干燥管E后再添加一个装有碱石灰的干燥管F。你认为是否需要添加F装置__________(填“需要”或“不需要”),简述理由________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。
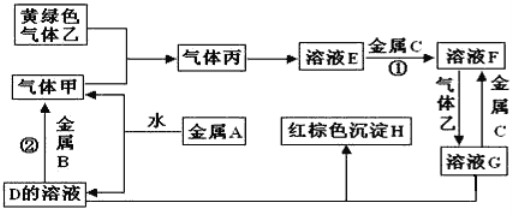
请根据以上信息回答下列问题
(1)写出下列物质的化学式:A__;H ___; G____;乙___。
(2)写出下列反应的化学方程式:
反应①_______;
反应②________。
(3)检测溶液G中金属离子的常用方法是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.Fe2O3(s) ![]() Fe(s)
Fe(s)![]() FeCl2 (s)
FeCl2 (s)
B.Cu2S(s) ![]() Cu(s)
Cu(s) ![]() CuSO4 (aq)
CuSO4 (aq)
C.Al(s)![]() NaAlO2 (aq)
NaAlO2 (aq) ![]() Al(OH)3(s)
Al(OH)3(s)
D.NaCl(aq) ![]() NaHCO3 (s)
NaHCO3 (s) ![]() Na2CO3 (s)
Na2CO3 (s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蓝色钾盐水合物KaCub(C2O4)c·H2O(铜元素为+2价)的组成可通过下列实验确定:
步骤①:称取一定质量的样品置于锥形瓶中,加入适量2 mol·L-1稀硫酸,微热使样品溶解。再加入30 mL水加热,用0.0200 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液12.00 mL(![]() 的还原产物为Mn2+)。
的还原产物为Mn2+)。
步骤②:充分加热滴定后的溶液,冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI,发生反应2Cu2++4I-=2CuI↓+I2
步骤③:加入少量淀粉溶液作指示剂,用0.0200 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液15.00 mL,发生反应I2+2![]() =2I-+
=2I-+![]()
(1)若步骤②中未对滴定后的溶液进行加热,则测出的Cu2+的物质的量将____(填“偏大”、“偏小” 或“不变”) 。
(2)步骤③中滴定终点的现象是___________。
(3)通过计算确定a:b:c=___________。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分离和提纯的方法错误的是
A.除去MgCl2溶液中的少量FeCl3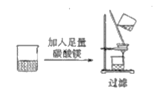
B.分离碘粉和铁粉的混合物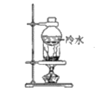
C.除去NaCl中的少量KNO3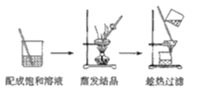
D.分离砂子、鸡蛋清和葡萄糖溶液的混合物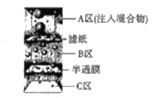
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新冠肺炎疫情期间,多种含氯消毒剂如84消毒液、Cl2、NaClO2等对病毒均具有很好的消杀作用,其中亚氯酸钠(NaClO2)在工业上常以ClO2气体为原料制备,实验室制备亚氯酸钠的装置如图所示(夹持装置已略)。
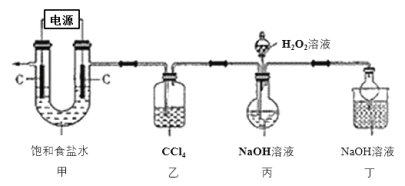
已知:①控制电压电解饱和食盐水可得到ClO2;
②Cl2易溶于CCl4;
③亚氯酸钠在不同温度下的溶解度如下表所示:
温度℃ | 20 | 40 | 60 |
溶解度/g | 6.2 | 23.4 | 48.3 |
回答下列问题:
(1)装置甲中产生ClO2的电极反应式为_____________________。
(2)装置乙中CCl4的作用为________________________________。
(3)装置丙中生成NaClO2的化学方程式为____________________________。
(4)从装置丙反应后的溶液中获得NaClO2晶体的步骤如下:
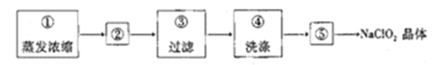
其中步骤①加热到_________________(填现象)时停止加热,步骤②是__________________。
(5)准确称取2.26gNaClO2粗品,加入盛有20.00mL刚煮沸并冷却过的水、足量10%的稀硫酸和30.00mL质量分数为40%的KI溶液(足量)的碘量瓶中,立即密封并摇晃碘量瓶至试样完全反应,再加入淀粉作指示剂用浓度为3.00mol/L的Na2S2O3溶液滴定(已知整个过程中发生的反应依次为![]() +4I-+4H+=2I2+Cl-+2H2O,
+4I-+4H+=2I2+Cl-+2H2O,![]() ),
),
①若三次平行实验测得消耗的Na2S2O3溶液的平均体积为30.00mL,则粗品的纯度为_________________%(保留三位有效数字),
②若使用的水未煮沸,则测定结果会___________________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A.按系统命名法,化合物![]() 的名称为2-甲基-4-乙基戊烷
的名称为2-甲基-4-乙基戊烷
B.苯酚、水杨酸(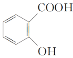 )和苯甲酸都是同系物
)和苯甲酸都是同系物
C.等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次减少
D.三硝基甲苯的分子式为C7H3N3O6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com