
| A. | 常温下,23g NO2含有NA 个氧原子 | |
| B. | 1 L 0.1 mol/L NaHSO3溶液中含有的HSO3-数目为0.1 NA | |
| C. | 1 L pH=1 的硫酸溶液中含有的H+ 数为0.2 NA | |
| D. | 标准状况下,2.24 L CO 和CO2混合气体中含有的氧原子数为0.15NA |
分析 A、求出二氧化氮的物质的量,然后根据二氧化氮的中含2个氧原子来分析;
B、HSO3-在溶液中既能电离又能水解;
C、pH=1的硫酸溶液中氢离子浓度为0.1mol/L;
D、CO和二氧化碳中含有的氧原子个数不同.
解答 解:A、23g二氧化氮的物质的量为0.5mol,而二氧化氮的中含2个氧原子,故0.5mol二氧化氮中含NA个氧原子,故A正确;
B、HSO3-在溶液中既能电离又能水解,故溶液中HSO3-的个数小于0.1NA个,故B错误;
C、pH=1的硫酸溶液中氢离子浓度为0.1mol/L,故1L溶液中氢离子的物质的量为n=CV=0.1mol/L×1L=0.1mol,个数为0.1NA个,故C错误;
D、标况下2.24L混合气体的物质的量为0.1mol,而CO和二氧化碳中含有的氧原子个数不同,故0.1mol混合气体中含有的氧原子个数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源: 题型:选择题
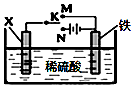
| A. | 若X为锌棒,开关K置于M处,为外加电流阴极保护法 | |
| B. | 若X为碳棒,开关K置于N处,为牺牲阳极阴极保护法 | |
| C. | 若X为锌棒,开关K置于M处,Zn极发生:Zn-2e-→Zn2+ | |
| D. | 若X为碳棒,开关K置于N处,X极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | 元素X、Y组成的化合物只有两种 | |
| C. | W的简单气态氢化物的热稳定性比Y的弱 | |
| D. | Q、Z的简单离子具有相同的电子层结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | b极发生还原反应 | |
| B. | a极的电极反应:CH3OH+H2O-6e-═CO2+6H+ | |
| C. | 总反应方程式为:2CO2+4H2O$\frac{\underline{\;通电\;}}{\;}$2CH3OH+3O2 | |
| D. | 该装置将化学能转变为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
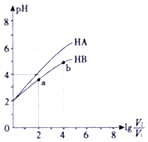 在25℃下,稀释HA、HB两种酸溶液,浓液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,下列说法不正确的是( )
在25℃下,稀释HA、HB两种酸溶液,浓液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,下列说法不正确的是( )| A. | a、b两点水的电离程度a小于b | |
| B. | HA、HB两种酸溶液pH相同时,c(HA)<c(HB) | |
| C. | 曲线上a、b两点$\frac{c({B}^{-})}{c(HB)•(O{H}^{-})}$一定相等 | |
| D. | 25℃时,NaA溶液中c(A-)一定大于NaB溶液中c(B-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式符合C4H8的同分异构体有4种 | |
| B. | 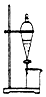 用如图所示装置完成用水除去硬脂酸钠中的甘油 | |
| C. | 乙醇的沸点高于丙烷,氨气的沸点高于磷化氢,都是因为分子间存在氢键 | |
| D. | 苯酚有毒,对皮肤有腐蚀性,若不慎沾到皮肤上,应立即用水洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾和漂白粉常用于自来水的净化,且原理相同 | |
| B. | 绚丽缤纷的烟花中添加了含钾、钠、铁、铜等金属元素的化合物 | |
| C. | 食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质 | |
| D. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com