
短周期主族元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为14。Y和Z位于同一周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的2倍。下列说法不正确的是
A.X的氢化物溶液与其最高价氧化物对应的水化物溶液的酸碱性相反
B.Y的氧化物既可与强酸反应又可与强碱反应,并可用来制作耐火材料
C.X和Y的最高价氧化物对应的水化物都是强酸
D.Z的氢化物与X的氢化物能够发生化学反应
C
【解析】
试题分析:Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的2倍,则Z的最外层电子数是6的倍数,所以Z的最外层电子数是6,则X的内层电子数是2,Y的最外层电子数是3,三种元素的最外层电子数之和是14,所以X的最外层电子数是14-6-3=5,则X是N元素,Y、Z则是第三周期元素,Y是Al元素,Z是S元素。A、X的氢化物是氨气,其水溶液呈碱性,最高价氧化物的水化物是硝酸,其水溶液呈酸性,酸碱性相反,正确;B、Al的氧化物氧化铝是两性氧化物,熔点较高,与强酸反应又可与强碱反应,并可用来制作耐火材料,正确;C、Y对应的最高价氧化物的水化物是氢氧化铝,属于两性氢氧化物,不是强酸,错误;D、S 氢化物是硫化氢,N的氢化物是氨气,二者可反应生成硫化铵,正确,答案选C。
考点:考查元素的推断,物质性质的判断


科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列物质的系统命名中,错误的是
A. 2,4-二甲基己烷
2,4-二甲基己烷
B.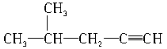 2-甲基-4-戊炔
2-甲基-4-戊炔
C.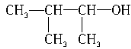 3-甲基-2-丁醇
3-甲基-2-丁醇
D.CH3—CHBr—CHBr—CH3 2,3-二溴丁烷
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市高二下学期学业水平模拟化学试卷(解析版) 题型:选择题
下列化学用语表达正确的是
A.乙酸的结构简式:C2H4O2 B.氢氧化钠的电子式: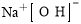
C.Cl-离子的结构示意图: D.NaClO的电离方程式:NaClO=Na++Cl-+O2-
D.NaClO的电离方程式:NaClO=Na++Cl-+O2-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市四校高三3月联合考试理综化学试卷(解析版) 题型:选择题
下列离子方程式或化学方程式与所述事实相符且正确的是
A.向0.1 mol/L、pH=1的NaHA溶液中加入NaOH溶液:H++OH- = H2O
B.以金属银为阳极电解饱和NaCl溶液:2Cl-+2H2O H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.硫酸与氢氧化钡反应的中和热化学反应方程式为:1/2 H2SO4(aq)+1/2 Ba(OH)2(aq) = 1/2 BaSO4(s)+H2O(l) ΔH=-57.3 kJ/mol
D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-= AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:填空题
(12分,每空2分)
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
(1)在一定体积的恒容密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g);△H<0
其化学平衡常数K与温度t的关系如下表,根据下表完成下列问题:
t/K | 298 | 398 | 498 | … |
K/(mol·L-1)2 | 4.1×106 | K1 | K2 | … |
①比较K1、K2的大小:K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆)
B.混合气体中氢气的质量不变
C.容器内压强保持不变
D.混合气体的密度保持不变
③某温度下,在一个10L的固定容器中充入2molN2和4molH2进行如下反应 N2(g)+3H2(g) 2NH3(g);△H<0一段时间达平衡后,N2的转化率为50%,求该温度下的平衡常数K= (mol/L)-2 ,平衡时NH3的体积分数为 。
(2)①肼(N2H4)高效清洁的火箭燃料。8g气态肼在氧气中完全燃烧生成氮气和气态水,放出133.5kJ热量,则肼燃烧的热化学方程式为 。
②盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,则盐酸肼中含有的化学键类型有 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
下列说法正确的是
A.c(H+)>c(OH-)的溶液一定显酸性
B.常温下,pH = 6 的溶液一定是酸溶液
C.电解稀硫酸或氢氧化钠溶液的产物不同
D.将纯水加热,其KW增大而pH不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为
A.蒸馏水、氨水、乙醇、二氧化硫 B.胆矾、空气、硫酸钠、干冰
C.生铁、盐酸、浓硫酸、碳酸钙 D.生石灰、漂白粉、氯化铜、硫酸钡
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:选择题
密闭容器中,发生反应:CO(g)+2H2(g)  CH3OH(g) ΔH<0,下列说法正确的是
CH3OH(g) ΔH<0,下列说法正确的是
A.一定温度下,压缩容器体积,则正反应速率加快,逆反应速率减慢
B.若甲醇的生成速率等于一氧化碳的消耗速率,则该反应达到平衡状态
C.升高温度,重新达到平衡时, 增大
增大
D.使用催化剂,反应的平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省仙桃天门潜江高三上学期期末联考理综化学试卷(解析版) 题型:填空题
(15分)(一)尿素又称碳酰胺,是含氮量最高的氮肥,工业上利用二氧化碳和氨气在一定条件下合成尿素。其反应分为如下两步:
第一步:2NH3(l)+CO2(g)  H2NCOONH4(氨基甲酸铵) (l) △H1= -330.0 kJ·mol-1
H2NCOONH4(氨基甲酸铵) (l) △H1= -330.0 kJ·mol-1
第二步:H2NCOONH4(l)  H2O(l)+H2NCONH2(l) △H2= + 226.3 kJ·mol-1
H2O(l)+H2NCONH2(l) △H2= + 226.3 kJ·mol-1
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 m3 密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
②反应进行到10 min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)= mol/(L·min)。
③当反应在一定条件下达到平衡,若在恒温、恒容下再充入一定量气体He,则CO(NH2)2(l)的质量_______(填“增加”、“减小”或“不变”)。
(二)氨是制备尿素的原料,氨气溶于水得到氨水,在25℃下,将a mol/L的氨水与b mol/L的硫酸以3∶2体积比混合反应后溶液呈中性。用含a和b的代数式表示出氨水的电离平衡常数为_________。此溶液中各离子浓度由大到小的顺序为_________。
(三)氢气是合成氨的原料。“氢能”将是未来最理想的新能源。
(1)在25℃,101KPa条件下,1 g氢气完全燃烧生成液态水时放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为 。
(2)氢气通常用生产水煤气的方法制得。其中C(s)+ H2O(g)  CO(g)+H2(g),在850℃时平衡常数K=1。若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H2O。
CO(g)+H2(g),在850℃时平衡常数K=1。若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H2O。
①当加热到850℃反应达到平衡的标志有______________ 。
A.容器内的压强不变
B.消耗水蒸气的物质的量与生成CO的物质的量相等
C.混合气的密度不变
D.单位时间有n个H—O键断裂的同时有n个H—H键断裂
②x应满足的条件是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com