
| A. | 尽管NO2能与水反应生成硝酸,但 NO2不属于酸性氧化物 | |
| B. | Na2O 溶于水所得溶液能导电,据此可判断 Na2O属于电解质 | |
| C. | 氨气和氯化氢气体混合后生成的NH4Cl是离子化合物,因此该反应为离子反应 | |
| D. | 某气体只含N、H 两种元素,且质量之比为14:3,则该气体一定为纯净物 |
分析 A.酸性氧化物是指和碱反应生成盐和水的氧化物,发生的反应为复分解反应,没有一种含N的酸中的N的化合价与NO2相同,NO2不属于酸性氧化物;
B.溶于水或熔融状态导电的化合物为电解质,化合物能本身电离出离子的化合物为电解质;
C.离子反应一定要在溶液中发生;
D.某气体只含N、H 两种元素,且质量之比为14:3可能是NH3,也可能是N2和H2的混合气体;
解答 解:A.NO2能与水反应生成硝酸是发生的氧化还原反应,没有一种含N的酸中的N的化合价与NO2相同,NO2不属于酸性氧化物,故A正确;
B.Na2O 溶于水所得溶液能导电,是因为氧化钠和水反应生成了氢氧化钠是电解质溶液中电离出自由移动的离子,溶液导电,但不能据此可判断 Na2O属于电解质,只有固体在熔融状态下导电可以判断氧化钠属于电解质,故B错误;
C.离子反应一定要在溶液中发生,故氨气和氯化氢气体的反应是气体反应不是离子反应,故C错误;
D.某气体只含N、H 两种元素,且质量之比为14:3,物质的量之比=$\frac{14}{14}$:$\frac{3}{1}$=1:3可能是NH3,也可能是N2和H2的混合气体,不一定是纯净物,故D错误;
故选A.
点评 本题考查了物质分类方法,物质组成特点,主要是酸性氧化物、离子反应的分析判断,掌握实质是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 常温下,铁比铝更易生锈,说明铁比铝活泼 | |
| B. | 钠比铜活泼,将钠投入硫酸铜溶液中,会有红色的铜析出 | |
| C. | 镁粉中混有的少量铝粉,可加足量NaOH溶液过滤除去 | |
| D. | 从1L 0.5mol/L FeCl3溶液中取出100mL,其中Cl-浓度为0.15 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
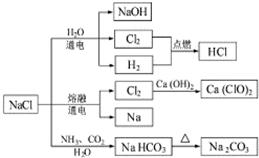 NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )
NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )| A. | 25℃时,NaHCO3在水中的溶解度比Na2CO3的小 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下液氯能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| C. | 在合成氨的反应中,降温或加压有利于氨的合成 | |
| D. | H2、I2、HI平衡混合气加压后颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液加入盐酸,有无色无味气体产生 | 溶液一定含有CO32- |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液一定含Fe2+ |
| C | 向某溶液滴加浓NaOH溶液加热,有能使湿润的红色石蕊试纸变蓝的气体产生 | 溶液一定存在NH4+ |
| D | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管中有晶体凝结 | NH4Cl固体可以升华 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com