
 .
. 与Br2,要想得到纯净的产物,可用NaOH溶液(或水)试剂洗涤.洗涤后分离粗产品应使用的仪器是分液漏斗.
与Br2,要想得到纯净的产物,可用NaOH溶液(或水)试剂洗涤.洗涤后分离粗产品应使用的仪器是分液漏斗. .
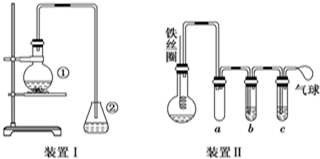
.分析 (1)溴与铁反应生成溴化铁,苯和液溴在溴化铁的催化作用下生成溴苯和溴化氢;溴离子与银离子生成了溴化银沉淀;
(2)长导管让挥发出来的溴单质冷凝,防止对产物的干扰;
(3)反应生成的溴苯和溴互溶呈红褐色油状液滴,可用NaOH溶液试剂洗涤,让反应生成溶于水的物质,再进行分液;
(4)支管是短进短出a的作用是防止倒吸安全装置;b中要除去Br2,b中试剂为苯或四氯化碳.
解答 解:(1)因溴与铁反应生成溴化铁:2Fe+3Br2 ═2FeBr3,苯和液溴在溴化铁的催化作用下生成溴苯和溴化氢: ;②中反应的离子方程式为Br-+Ag+═AgBr↓,
;②中反应的离子方程式为Br-+Ag+═AgBr↓,
故答案为:2Fe+3Br2═2FeBr3, ;Br-+Ag+═AgBr↓;
;Br-+Ag+═AgBr↓;
(2)反应为放热反应,长导管让挥发出来的溴单质冷凝,防止对产物的干扰,即长导管的作用为导气,冷凝回流,故答案为:导气,冷凝回流;
(3)反应生成的溴苯和溴互溶呈红褐色油状液滴,可用NaOH溶液试剂洗涤,让反应生成溶于水的物质,再进行分液,
故答案为: 与Br2;NaOH溶液(或水);分液漏斗;
与Br2;NaOH溶液(或水);分液漏斗;
(4)从图上信息可知,支管是短进短出a的作用是防止倒吸安全装置;B中要除去Br2,试剂为苯或四氯化碳,该装置的优点是:可以控制反应进行;避免杂质干扰;防止污染空气,
故答案为:防止倒吸;CCl4或 ;可以控制反应进行,避免杂质干扰,防止污染空气.
;可以控制反应进行,避免杂质干扰,防止污染空气.
点评 本题考查制备实验,为高频考点,把握溴苯的制备、混合物分离提纯、实验装置的作用等为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
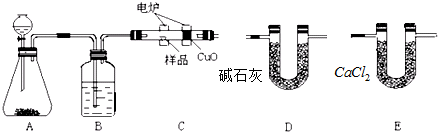
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
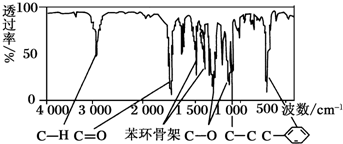
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3、Fe2O3均为两性氧化物 | |
| B. | 该反应中化学能全部转化为热能 | |
| C. | Al2O3中的微粒半径:r(Al3+)>r(O2-) | |
| D. | 在该反应条件下,Al的还原性强于Fe的还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
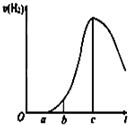 某化学小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断.将5.4g铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产氢速率与反应时间的关系图.
某化学小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断.将5.4g铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产氢速率与反应时间的关系图.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
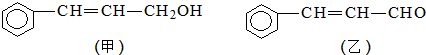
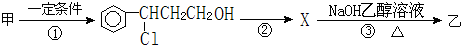
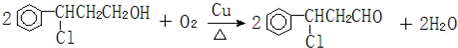 (注明反应条件).
(注明反应条件).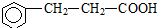 ).写出同时符合下列要求的丙的同分异构体结构简式
).写出同时符合下列要求的丙的同分异构体结构简式 、
、 ,.
,.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
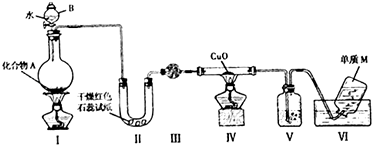
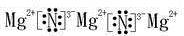 ,A与水反应的化学方程式Mg3N2 +6H2O=3Mg(OH)2↓+2NH3↑,比较A中阴阳离子的大小,阳离子半径小于阴离子半径(填大于,小于或等于)
,A与水反应的化学方程式Mg3N2 +6H2O=3Mg(OH)2↓+2NH3↑,比较A中阴阳离子的大小,阳离子半径小于阴离子半径(填大于,小于或等于)查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com