
| A�� | Na2SO4�� NaCl �����ʵ���֮��Ϊ 1��3 | |
| B�� | ��Һ��һ���� 1molNa2SO4 �� 3molNaCl | |
| C�� | ��������� SO42-�� Na+�� $\frac{3}{5}$ �� | |
| D�� | SO42-�� Cl-�����ʵ���֮�͵��� Na+�����ʵ��� |
���� �ڻ����Һ�д��ڵ���غ㣺c��Cl-��+2c��SO42-��=c��Na+����Cl-�����ʵ���Ũ����Na+�����ʵ���Ũ�ȵ�$\frac{3}{5}$������c��Na+��=5mol/L����c��Cl-��=3moL/L��c��SO42-��=1mol/L���Դ˽��
��� �⣺�ڻ����Һ�д��ڵ���غ㣺c��Cl-��+2c��SO42-��=c��Na+����Cl-�����ʵ���Ũ����Na+�����ʵ���Ũ�ȵ�$\frac{3}{5}$������c��Na+��=5mol/L����c��Cl-��=3moL/L��c��SO42-��=1mol/L��
A����c��Cl-��=3moL/L����c��SO42-��=1mol/L����Na2SO4 ��NaCl�����ʵ���֮��Ϊ1��3����A��ȷ��
B����Һ���δ֪������n=CV��֪����ȷ�������ƺ��Ȼ��Ƶ����ʵ�������B����
C����c��Na+��=5mol/L����c��SO42-��=1mol/L�����������SO42-��Na+��$\frac{2}{5}$������C����
D�����ݵ���غ㣺c��Cl-��+2c��SO42-��=c��Na+����SO42- ��Cl-�����ʵ���֮��С����Na+�����ʵ�������D����
��ѡ��A��
���� ���⿼�����ʵ���Ũ�ȵ��йؼ��㣬�ѶȲ��ؼ�������Һ�ʵ����ԣ����������������������ȣ�


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ӱ�컯ѧ��Ӧ���ʵı������� | |
| B�� | ����Ӧ��ϵ�ݻ�����ʱ����С��Ӧ������϶��ܽ��ͷ�Ӧ���� | |
| C�� | ���淴Ӧ�ﵽ��Ӧ��ʱ����ѧ��Ӧ����Ϊ0 | |
| D�� | ��ѧ��Ӧ���ʿ��õ�λʱ���ڷ�Ӧ���Ũ�ȱ仯������ʾ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϴ���ļ����Ǽ������һ��ϴ��Һ���Ƿ����γɳ����ĸ���Һ�е����� | |
| B�� | ϴ�ӵ��Լ�һ���ѡ������ˮ����ˮ���Ҵ��������ʵı�����Һ | |
| C�� | ϴ�ӵ�Ŀ��һ���dz�ȥ���������������Ե����ʣ���ߴ��� | |
| D�� | ϴ�ӵIJ���������������ϴ�Ӽ���һ��ϴ�Ӽ�������ӣ�Ȼ����ϴ�Ӽ���Ȼ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��Na+��NO3-��Br- | B�� | Na+��NH4+��NO3-��Cl- | ||
| C�� | K+��Na+��HCO3-��NO3- | D�� | K+��Cu2+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5.6 g Fe ��������������ȫȼ��ʧȥ������Ϊ 3N A | |
| B�� | 1L Ũ��Ϊ 0.5mol/LFeCl3 ��Һ������к����� 0.5molFe��OH��3�������� | |
| C�� | ���³�ѹ�£�23 g NO2 �� N2O4 �Ļ������һ������ N A ����ԭ�� | |
| D�� | ����£�4.48L ��ˮ�к��� H2O ���ӵ���ĿΪ 0.2N A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
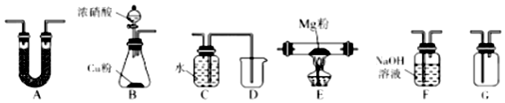
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
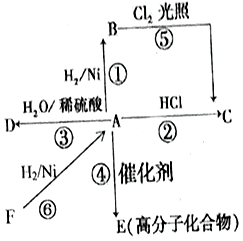 ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ��
ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com