
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是

A. 原子半径Y<Z<W
B. 元素Y的最高正化合价比元素X的最高正化合价高
C. 元素W的最高价氧化物对应的水化物的酸性比Q的弱
D. 元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性
科目:高中化学 来源: 题型:
【题目】氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知: 氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。
I.制备氢化锂
选择图I中的装置制备氢化锂(有些装置可重复使用):
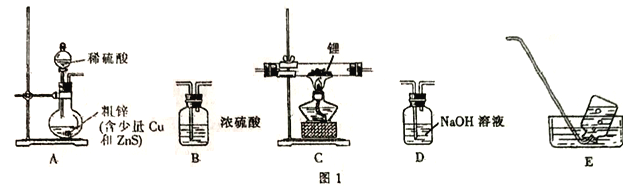
(1)装置的连接顺序(从左至右)为A→______________。
(2)检在好装蹬装置的气密性,点燃酒精灯前需进行的实验操作是_______________。
(3)写出制备氢化铝锂的化学方程式:__________________。
II. 制备氢化铝锂
1947年,Schlesinger,Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅样,充分反应后,经一系列操作得到LiAlH4晶体。

(4)写出氢化锂与无水三氯化铝反应的化学方程式:____________________。
III.测定氢化铝锂产品(不含氢化锂)的纯度
(5)按图2装配仪器、检查装置气密性并装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是________。读数之前上下移动量气管右侧的容器,使量气管左、右有两侧的液面在同一水平面上,其目的是_________。
(6)在标准状况下,反应前量气管读数为V1mL,反应完毕并冷却之后,量气管读数为V2mL。该样品的纯度为_____________(用含a、V1、V2的代数式表示)。如果起始读数时俯视刻度线,测得的结果将________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
I.现有反应:①![]() ,②
,②![]() 。
。
(1)两反应中属于吸热反应的是______![]() 填序号
填序号![]() 。
。
(2)![]() 原电池的装置如图所示。
原电池的装置如图所示。
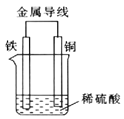
①溶液中![]() 向______
向______![]() 填“铁”或“铜”
填“铁”或“铜”![]() 电极方向移动。
电极方向移动。
②正极的现象是______,负极的电极反应式为______。
![]() 某可逆反应:
某可逆反应:![]() 在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 |
|
|
|
|
|
| |
2 | 800 |
|
|
|
|
|
|
|
3 | 950 |
|
|
|
|
|
|
|
(3)实验1中,在![]() min内,以物质A表示的平均反应速率为______
min内,以物质A表示的平均反应速率为______![]() ,50min时,
,50min时,![]() 正
正![]() ______
______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 逆
逆![]() 。
。
(4)0~20min内,实验2比实验1的反应速率______![]() 填“快”或“慢”
填“快”或“慢”![]() ,其原因可能是______。
,其原因可能是______。
(5)实验3比实验1的反应速率快,其原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列化合物的名称或结构简式:
(1)结构简式为 的烃可命名为:________________________________。
的烃可命名为:________________________________。
(2)结构简式为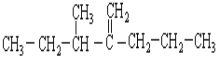 此烃名称为____________________________。
此烃名称为____________________________。
(3)2,5-二甲基-2,4-己二烯 的结构简式:__________________________。
(4)有机物 的系统名称为________________
的系统名称为________________
(5)结构简式  的烃可命名为___________________。
的烃可命名为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F都是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1mol·L-1D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法不正确的是
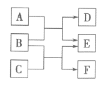
A. B晶体中阴、阳离子个数比为1:2
B. 等体积等浓度的F溶液与D溶液中,阴离子总的物质的量F>D
C. 0.1molB与足量A或C完全反应转移电子数均为0.1NA
D. Y、Z分别形成的简单氢化物的稳定性前者弱于后者,是因为后者分子间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() 、
、![]() 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素,![]() 为地壳中含量最高的过渡金属元素,
为地壳中含量最高的过渡金属元素,![]() 与
与![]() 同主族,
同主族,![]() 与
与![]() 同周期,且
同周期,且![]() 与
与![]() 的原子序数之和为20,
的原子序数之和为20,![]() 单质能与无色无味液体
单质能与无色无味液体![]() 反应置换出
反应置换出![]() 单质,
单质,![]() 单质也能与
单质也能与![]() 反应置换出
反应置换出![]() 单质,
单质,![]() 、
、![]() 、
、![]() 均能与
均能与![]() 形成离子化合物,下列说法不正确的是( )
形成离子化合物,下列说法不正确的是( )
A. ![]() 、
、![]() 两元素的形成的化合物都为黑色固体
两元素的形成的化合物都为黑色固体
B. ![]() 、
、![]() 形成的离子化合物可能含有其价键
形成的离子化合物可能含有其价键
C. ![]() 的单质只有还原性,没有氧化性
的单质只有还原性,没有氧化性
D. 工业上可以用铝热法制取金属![]() 用于野外焊接铁轨
用于野外焊接铁轨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2S是一种二元弱酸,回答以下问题:
(1)0.1mol/L NaHS溶液显碱性,则c(S2-)___________c(H2S)(填“大于” ,“小于” 或“等于” ) 。
(2)已知常温下,CaS饱和溶液中存在平衡:CaS(s)![]() Ca2+(aq)+S2-(aq) ΔH>0。
Ca2+(aq)+S2-(aq) ΔH>0。
①温度升高时,Ksp________ (填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)________,原因是__________________________________(用文字和离子方程式说明)。
(3)若向CaS悬浊液中加入Cu(NO3)2溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
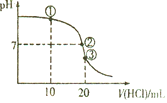
【题目】常温下,向20mL0.1mol/L氨水中逐滴加入0.1mol/L盐酸,测得溶液的pH随加入盐酸的体积变化如图所示。下列说法正确的是( )
A.①溶液中:c(Cl-)=2c(NH4+)+2c(NH3·H2O)
B.②溶液中:c(NH4+)= c(Cl-)= c(OH-)= c(H+)
C.③溶液中:c(H+)= c(OH-)+ c(NH4+)+c(NH3·H2O)
D.滴定过程中可能出现:c(NH3·H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:N2H4+O2=N2+H2O,下列关于该电池工作时的说法正确的是( )

A. 该装置工作时,Ag电极上有气体生成
B. 甲池中负极反应为N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均减小
D. 当甲池中消耗0.1molN2H4时,乙池中理论上最多产生6.4g固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com