
分析 配合物中內界原子不能发生电离,外界离子在水溶液里能发生电离,氯离子可以与银离子反应生成氯化银白色沉淀,根据沉淀情况可以得到有几个离子在配合物中,根据元素守恒及配合物的特点,确定化学式;根据CO32-的中心原子价电子对数确定离子的空间构型,价层电子对个数=σ键个数+孤电子对个数.
解答 解:在A中加入硝酸银溶液只有$\frac{1}{3}$的氯可被沉淀,说明在反应生成物中有$\frac{1}{3}$的氯在配合物的外界,又因为A的化学式为CoCl3H12N4,其中有氨分子和$\frac{2}{3}$的氯离子做配体,根据元素守恒及配合物的特点,可推知A的结构式为[Co(NH3)4Cl2]Cl;在CO32-的中孤对电子$\frac{4+2-3×2}{2}$=0,价层电子对个数=3+0=3,所以C按sp2方式杂化,其空间构型为正三角形,
故答案为:[Co(NH3)4Cl2]Cl; 正三角形.
点评 本题考查配合物和微粒的空间构型判断,注意配合物内界与外界区别:配合物中外界离子在水溶液里能发生电离,內界原子不能发生电离以及掌握价层电子对互斥理论的应用是解答关键,题目难度中等.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | i | |||||||||||||
| j | |||||||||||||||||
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据②③④可确定一定含有NO2-、CO32-、Cl-三种阴离子 | |
| B. | 由②中的实验现象可推测一定含有NO2- | |
| C. | 不能确定是否一定含有NO3- | |
| D. | 由④即可确定一定不存在SO42-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠的电离是指在电流作用下离解成钠离子和氯离子 | |
| B. | 溶于水后能电离出氢离子的化合物都是酸 | |
| C. | 硫酸钡难溶于水,所以硫酸钡属于弱电解质 | |
| D. | 醋酸溶液中存在H+、CH3COOH、CH3COO-等微粒,故醋酸是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
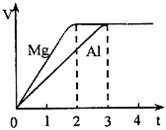 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )| A. | 反应消耗镁、铝的物质的量之比是3:2 | |
| B. | 反应消耗镁、铝的质量之比是3:2 | |
| C. | 与镁和铝反应的硫酸的物质的量之比是3:2 | |
| D. | 与镁和铝反应的硫酸的质量之比是3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com