
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.5 | 4.7 |
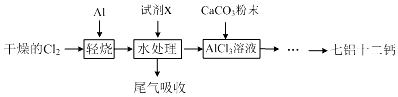
分析 由制备流程可知,Al与氯气加热反应生成AlC13,加试剂X为盐酸,可抑制氯化铝的水解,AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后锻烧沉淀制备七铝十二钙 (12CaO•7Al2O3).
(1)蒸气凝华为固体可堵塞导气管;
(2)氯化铝为强酸弱碱盐,可发生水解反应;
(3)要求n(CaCO3):n(A1C13)>12:14,与氢氧化钙的溶解性有关,用氨水沉淀、过滤后的滤液含铵根离子、氯离子;
(4)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12•2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水,将亚铁离子氧化为铁离子,结合表格中pH可知,调节pH为4.7,使Fe3+、Al3+完全转化为沉淀,过滤后,向滤液中加盐酸酸化,蒸发浓缩,冷却结晶,过滤,冰水洗涤,干燥得到CaC12•2H2O.
解答 解:(1)轻烧后的气体用水处理前导气管要保温是为了防止AlC13蒸气凝华堵塞导气管,
故答案为:为了防止AlC13蒸气凝华堵塞导气管;
(2)用水处理添加的试剂X是盐酸,其目的是抑制铝离子水解,
故答案为:盐酸;抑制铝离子水解;
(3)由于氢氧化钙微溶于水,钙元素会有损失,所以碳酸钙要适当过量,用氨水沉淀、过滤后的滤液含铵根离子、氯离子,则滤液主要成分是NH4Cl(少量CaCl2),
故答案为:氢氧化钙微溶于水,造成损失; NH4Cl(少量CaCl2);
(4)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12•2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水,加入氢氧化钙,搅拌,用pH计调节溶液的pH为4.7,过滤,向滤液中加盐酸酸化,蒸发浓缩,冷却结晶,过滤,冰水洗涤,干燥得到CaC12•2H2O,
故答案为:加入氢氧化钙,搅拌,用pH计调节溶液的pH为4.7,过滤;向滤液中加盐酸酸化,蒸发浓缩,冷却结晶,过滤.
点评 本题考查物质的制备实验,为高频考点,把握制备原理、发生的反应、盐类水解、混合物分离为解答的关键,侧重分析与实验能力的考查,注意氧化还原反应及表格中pH的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O(g)=H2(g)+$\frac{1}{2}$ O2(g)△H=+242 kJ/mol | B. | 2H2(g)+O2(g)=2H2O (l)△H=-484 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$ O2(g)=H2O (g)△H=-242 kJ | D. | 2H2(g)+O2(g)=2H2O (g)△H=+484 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解搅拌时有液体飞溅 | |
| B. | 取KMnO4样品时不慎在表面沾了点蒸馏水 | |
| C. | 定容时俯视容量瓶刻度线 | |
| D. | 定容摇匀后见液面下降,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室将硫酸铜溶液直接加热蒸干来制取CuSO4•5H2O | |
| B. | 用湿润的pH试纸来测溶液的pH | |
| C. | 不慎将浓碱溶液沾到皮肤上,可先立即用稀盐酸中和,后用大量水冲洗,再涂上2%~5%的硼酸溶液 | |
| D. | 用四氯化碳萃取溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com