
【题目】组成大熊猫和大肠杆菌细胞的最基本的化学元素和含量最多的化学元素依次是( )
A. C和O B. C和H C. O和C D. H和O
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)![]() 2Z(g)+W(s),该反应的ΔH<0,下列叙述正确的是
2Z(g)+W(s),该反应的ΔH<0,下列叙述正确的是
A.平衡常数K值越大,X的转化率越大
B.达到平衡时,反应速率v正(X)=2v逆(Z)
C.达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产、生活中产生的废水、废气是环境污染的重要源头。在环境治理方面人们可利用I2O5和Na2SO3等化工产品实现对废水和废气的治理。
(1)利用I2O5的氧化性处理废气H2S,得到S、I2两种单质,发生反应的化学方程式为________________。
(2)利用I2O5也可消除CO的污染,其反应原理为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s) ΔH。已知在不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
5CO2(g)+I2(s) ΔH。已知在不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
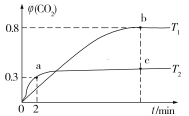
①温度为T2时,0~2 min 内,CO2的平均反应速率υ(CO2)=__________________。
②b点时CO的转化率为__________,化学反应的平衡常数K=_______(填表达式)。
③反应:I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)的ΔH______0(填“>”“<”或“=”)。
5CO2(g)+I2(s)的ΔH______0(填“>”“<”或“=”)。
④上述反应在T1下达到平衡时,再向容器中充入物质的量均为2 mol的CO和CO2气体,则化学平衡________(填“向左”“向右”或“不”)移动。
⑤下列现象,可以表示上述反应达到平衡状态的是____________(填字母)。
A.容器内的压强不再变化 B.混合气的平均相对分子质量不再变化
C.混合气的密度不再变化 D.单位时间内消耗CO和生成CO2的物质的量之比为1∶1
(3)Na2SO3具有还原性,其水溶液可以吸收Cl2(g),减少环境污染。
已知反应:①Na2SO3(aq)+Cl2(g)+H2O(l) ![]() Na2SO4(aq)+2HCl(aq) ΔH1=a kJ·mol1
Na2SO4(aq)+2HCl(aq) ΔH1=a kJ·mol1
②Cl2(g)+H2O(l) ![]() HCl(aq)+HClO(aq) ΔH2=b kJ·mol1
HCl(aq)+HClO(aq) ΔH2=b kJ·mol1
试写出Na2SO3(aq)与HClO(aq)反应的热化学方程式:________________________。
(4)某工业废水中含有Hg2+、Cu2+等离子。取一定量的该工业废水,向其中投入一定量的MnS固体,当CuS开始沉淀时,溶液中![]() =____________(结果保留两位有效数字)。
=____________(结果保留两位有效数字)。
[已知:Ksp(HgS)=6.4×1053,Ksp(CuS)=1.3×1036,Ksp(MnS)=2.5×1013。]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是天然气的主要成分,是一种重要的清洁能源和化工原料。
Ⅰ.煤制天然气时会发生多个反应,生产过程中有多种途径生产CH4。
已知:
① CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1
② C(s)+2H2(g)![]() CH4(g)ΔH=-73kJ·mol-1
CH4(g)ΔH=-73kJ·mol-1
③ 2CO(g)![]() C(s)+CO2(g)ΔH=-171kJ·mol-1
C(s)+CO2(g)ΔH=-171kJ·mol-1
写出CO2与H2反应生成CH4和H2O的热化学方程式____________________。
Ⅱ.新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液(滴有几滴酚酞)电解实验,如图所示:
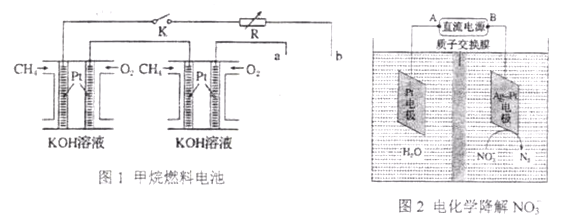
回答下列问题:
(1)①用甲烷燃料电池作为电化学降解NO3-装置的直流电源时,应将A与_____相连(填a或b,下同)B与_____相连。阴极反应式为_____________。
②若电解过程中转移了2mol电子,则膜的两侧电解液的质量变化差(Δm左- Δm右)为________g。
(2)甲烷燃料电池正极、负极的电极反应分别为________ 、_________。
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则图二电解池中理论上Pt最多能产生的氯气体积为________L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类的生产、生活、科技、航天等方面密切相关。下列说法正确的是
A.汝窑瓷器的天青色来自氧化铁
B.“傍檐红女绩丝麻”所描述的丝、麻主要成分是蛋白质
C.中国歼—20上用到的氮化镓材料是作为金属合金材料使用
D.诗句“煮豆燃豆萁”中涉及的能量变化主要是化学能转化为热能和光能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于下列事实的解释错误的是( )
A. 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B. 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C. 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
D. 浓硫酸常温下与铜不反应,加热时才能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】初中生小张正处于身体发育的快速增长期, 但其经常感觉到腿抽筋并有严重蛀牙, 他可能需要补充无机盐
A. Na+ B. Ca2+ C. Mg2+ D. Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g) H=+11 kJ·mol-1。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g) H=+11 kJ·mol-1。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示。当改变条件,再次达到平衡时,下列有关叙述不正确的是

A.若升高温度到某一温度,再次达到平衡时,相应点可能分别是A、E
B.若再次充入a mol HI,则达到平衡时,相应点的横坐标值不变,纵坐标值增大
C.若改变的条件是增大压强,再次达到平衡时,相应点与改变条件前相同
D.若改变的条件是使用催化剂,再次达到平衡时,相应点与改变条件前不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种溶液中:①pH值为0的盐酸;②0.lmol/L的盐酸;③0.01mol/L的氢氧化钠溶液;④pH值为11的氢氧化钠溶液。由水电离生成的c(H+)之比依次为
A. 0:1: 12:11 B. 14:13:12:11
C. 14:13:2:3 D. 1:10:100:1000
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com