
分析 (1)MnO2和浓盐酸加热反应生成氯气、氯化锰和水;
(2)利用刚吸收过少量SO2的NaOH溶液吸收含有氯气的尾气,根据溶液中发生的反应分析存在的阴离子;
①可假设1:只存在SO32-;假设2只存在ClO-;假设3:既不存在SO32-,也不存在ClO-;
②SO32-具有还原性,ClO-具有氧化性,二者不能共存;
③根据所限制实验试剂和SO32-、ClO-的性质,先加入硫酸至酸性,若存在SO32-、ClO-,分别生成了H2SO3和HClO;H2SO3具有还原性,选择具有强氧化性的高锰酸钾溶液,证明SO32-的存在;因为HClO具有强氧化性,紫色石蕊溶液,证明有ClO-的存在;
(3)首先计算SO2和NaOH的物质的量,判断反应产物,列方程式计算相关物理量;根据转移电子数相等来计算消耗KIO3溶液的体积.
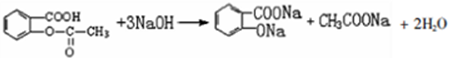
解答 解:(1)MnO2和浓盐酸加热反应生成氯气、氯化锰和水,其反应的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)利用刚吸收过少量SO2的NaOH溶液吸收含有氯气的尾气,少量的SO2与NaOH溶液反应生成Na2SO3,Na2SO3被氯气氧化生成硫酸钠,其反应方程式为Cl2+Na2SO3+2NaOH=2NaCl+Na2SO4+H2O,故一定存在SO42-、Cl-,
故答案为:SO42-、Cl-;
①由已知假设1、只存在SO32-,假设3、既存在SO32-也存在ClO-,可知假设2为为:只存在ClO-,
故答案为:只存在ClO-;
②SO32-具有强还原性,ClO-具有强氧化性,两者发生氧化还原反应而不能大量共存,
故答案为:SO32-具有强还原性,ClO-具有强氧化性,两者发生氧化还原反应而不能大量共存;
③因为吸收液呈碱性,先取少量吸收液于试管中,滴加3moL•L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中先加入硫酸的试管,若存在SO32-、ClO-,分别生成了H2SO3和HClO;在A试管中滴加0.01mol•L-1KMnO4溶液,若紫红色褪去,证明有SO32-,则说明假设1成立;在B试管中滴加紫色石蕊溶液,若溶液先变红后褪色,证明有ClO-,则说明假设2成立,
故答案为:紫色石蕊溶液;先变红后褪色;
(3)n (SO2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,n(NaOH)=0.015L×1mol/L=0.015mol,
则反应的可能方程式有:SO2+2NaOH=Na2SO3+H2O,SO2+NaOH=NaHSO3,
则有:2>$\frac{n(NaOH)}{n(SO{\;}_{2})}$=$\frac{3}{2}$>1,
所以:所得产物为Na2SO3和NaHSO3,
设所得产物中含Na2SO3为xmol,NaHSO3为ymol则得方程组:$\left\{\begin{array}{l}{x+y=0.01}\\{2x+y=0.015}\end{array}\right.$,解得:x=0.005,y=0.005,即正盐的物质的量为:0.005mol;
设0.2000mol•L-1 KIO3溶液VL恰好将上述溶液X中所有的硫元素氧化,还原产物为I2,则KIO3得电子总数为:0.2000mol/L×VL×(5-0),
X溶液中硫失电子总数为:0.01mol×(6-4),根据得失电子总数相等得:0.2000mol/L×VL×(5-0)=0.01mol×(6-4),解答V=20mL,
故答案为:0.005mol;20.
点评 本题属于实验探究题,要根据实验原理提出假设,再结合物质的性质加以验证,侧重于考查学生的实验探究能力和对知识的应用能力,题目难度中等.计算时注意先判断反应产物,利用氧化还原反应中转移电子数相等来计算可简化计算过程.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:填空题
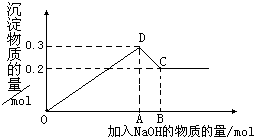 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉浮的物质的量(mol)的关系如图所示.则:
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉浮的物质的量(mol)的关系如图所示.则:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | ||||
| T | Q | W |
| A. | 工业电解熔融的 TW3制得单质T | |
| B. | 元素R和元素Q的最高正化合价相同 | |
| C. | 单核阴离子半径的大小顺序为r(Q)>r(W)>r(R) | |
| D. | 阴离子的还原性:Q<W |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C可用于文物的年代鉴定,14C与12C互为同素异形体 | |
| B. | 食用一定量的油脂能促进人体对某些维生素的吸收 | |
| C. | “血液透析”利用了胶体的性质 | |
| D. | 服用铬含量超标的药用胶囊会对人体健康造成危害 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除③外 | B. | 除③⑤外 | C. | 除③④外 | D. | 除⑥外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
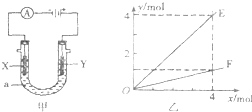 电解原理在化学工业中有着广泛的应用.图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.则下列说法不正确的是( )
电解原理在化学工业中有着广泛的应用.图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.则下列说法不正确的是( )| A. | 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 | |
| B. | 按图甲装置用惰性电极电解AgN03溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 | |
| C. | 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol | |
| D. | 若X、Y为铂电极.a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
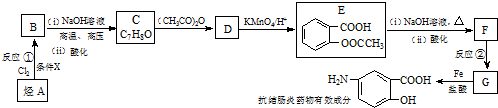
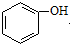 $\stackrel{(CH_{3}CO)_{2}O}{→}$
$\stackrel{(CH_{3}CO)_{2}O}{→}$ (b)
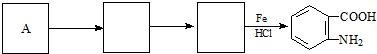
(b)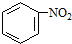 $→_{盐酸}^{Fe}$
$→_{盐酸}^{Fe}$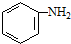
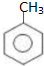 ;
; ;
;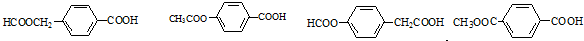 ;
;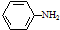 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代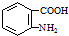 ) 合成路线中两种中间产物的结构简式(部分反应条
) 合成路线中两种中间产物的结构简式(部分反应条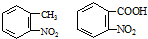 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com