
|
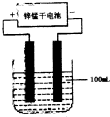
如下图,锌锰干电池在放电时总反应方程式可表示为Zn(s)+2MnO2+2
| |
| [ ] | |
A. |
Zn |
B. |
碳 |
C. |
MnO2和 |
D. |
Zn2+和NH3 |
科目:高中化学 来源: 题型:阅读理解


| ||
| ||


查看答案和解析>>
科目:高中化学 来源:导学大课堂必修二化学人教版 人教版 题型:021
|
如下图,锌锰干电池在放电时总反应方程式可表示为:Zn(s)+2MnO2+2
| |
A. |
Zn |
B. |
碳 |
C. |
MnO2和 |
D. |
Zn2+和NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

A.Zn B.碳 C.MnO2和![]() D.Zn2+和NH3
D.Zn2+和NH3
查看答案和解析>>
科目:高中化学 来源:同步题 题型:不定项选择题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com