
【题目】下列四种化合物中,不能与氢氧化钠溶液反应的是
A.碳铵(碳酸氢铵) B.二氧化硅 C.氧化铝 D.一氧化碳
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】已知:![]()
![]()
![]() 。25℃时,调节初始浓度为1.0 molL-1 的Na2CrO4溶液的pH,测定平衡时溶液中c(
。25℃时,调节初始浓度为1.0 molL-1 的Na2CrO4溶液的pH,测定平衡时溶液中c(![]() )和c(H+),获得如右图所示的曲线。下列说法不正确的是
)和c(H+),获得如右图所示的曲线。下列说法不正确的是
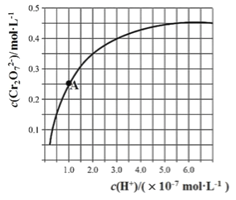
A.平衡时,pH越小,c(![]() )越大
)越大
B.A点CrO![]() 的平衡转化率为50%
的平衡转化率为50%
C.A点CrO![]() 转化为
转化为![]() 反应的平衡常数K=1014
反应的平衡常数K=1014
D.平衡时,若溶液中c(![]() )=c(
)=c(![]() ),则c(H+) > 2.0×10-7 mol·L-1
),则c(H+) > 2.0×10-7 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由 。
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
(6)实验时所用盐酸及NaOH溶液的密度均为1g/cm3,生成溶液的比热容C=4.18J/(g·℃),实验起始温度为t1℃,终止温度为t2℃。试推断中和热的计算式:△H=____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成分为Fe(CrO2)2]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:

已知:铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,且Al2O3+Na2CO3![]() 2NaAlO2+CO2↑。请回答:
2NaAlO2+CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为 。
(2)滤渣2的成分为 。
(3)将滤渣1放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是 。
(4)根据有关国家标准,含CrO![]() 的废水要经化学处理,使其浓度降至5.0×10-7 mol/L以下才能排放。含CrO
的废水要经化学处理,使其浓度降至5.0×10-7 mol/L以下才能排放。含CrO![]() 的废水处理通常用以下方法:还原法:
的废水处理通常用以下方法:还原法:![]() 。写出酸性条件下CrO
。写出酸性条件下CrO![]() 与绿矾(FeSO4.7H2O)在溶液中反应的离子方程式:____________________________。
与绿矾(FeSO4.7H2O)在溶液中反应的离子方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算题:将等物质的量的A 和B混合于2L密闭容器中,发生下列反应:
3A(g)+B(g)=xC(g)+2D(g),4min后测得c(D)=0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.125mol/(L·min),求:(1)x的值是多少?(2)此时A的物质的量浓度?(3)B的平均反应速率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生反应:3A(g)+B(g) ![]() xC(g)Ⅰ.将3mol A和2mol B,在一定条件下反应,达到平衡时C的体积分数为a;Ⅱ.若A、B、C起始投入的物质的量分别为n(A)、n(B)、n(C),在相同条件下达到平衡时,C的体积分数也为A.下列有关叙述正确的是
xC(g)Ⅰ.将3mol A和2mol B,在一定条件下反应,达到平衡时C的体积分数为a;Ⅱ.若A、B、C起始投入的物质的量分别为n(A)、n(B)、n(C),在相同条件下达到平衡时,C的体积分数也为A.下列有关叙述正确的是
A.若Ⅰ达到平衡时,A、B、C各增加1mol,则B的转化率一定增大
B.若向平衡Ⅰ中再加入6mol A,4mol B.测得C的体积分数大于a,可断定x>4
C.若x=2,则体系Ⅱ起始物质的量应满足:3n(B)=n(A)-3
D.若体系Ⅱ起始物质的量满足3n(c)+4nA=12nB,则可推断:x=4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从生物学的角度,下列几则广告语科学的是( )
A. 加碘食盐对人健康很重要,碘是人体必需的元素
B. 这种口服液含有丰富的钙、铁、锌、硒等微量元素
C. 吃生鸡蛋更有利于人体消化,利于身体健康
D. 这种营养品含有人体所需的全部20种必需氨基酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com