
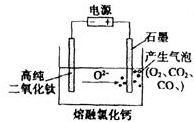
 如图为EFC剑桥法用固体二氧化钛(TiO2)生产海绵钛的装置示意图,其原理是在较低的阴极电位下,TiO2(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛.阴极的电极反应式为TiO2+4e-→Ti+2O2-,石墨电极的质量是否发生变化是 (填“是”或“否”).
如图为EFC剑桥法用固体二氧化钛(TiO2)生产海绵钛的装置示意图,其原理是在较低的阴极电位下,TiO2(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛.阴极的电极反应式为TiO2+4e-→Ti+2O2-,石墨电极的质量是否发生变化是 (填“是”或“否”). 科目:高中化学 来源: 题型:选择题
| A. | 在氯化铝溶液中滴加氨水 | B. | 在偏铝酸钠溶液中通入CO2 | ||
| C. | 在氯化铝溶液中滴加氢氧化钠溶液 | D. | 在硫酸铝溶液中滴加偏铝酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol Cl2 | |
| B. | 标准状况下3.36 L CO | |
| C. | 5.6g N2 (N2的摩尔质量为28 g•mol-1) | |
| D. | 含NA个分子的O2(NA为阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把SiO2加入到NaOH溶液中:SiO2+2OH-═SiO32-+H2O | |
| B. | 向NaHCO3溶液中滴入NaOH溶液:HCO3-+OH-═CO2↑+H2O | |
| C. | 向Al(OH)3中滴入H2SO4溶液:Al(OH)3+3H+═Al3++3H2O | |
| D. | 向Na2CO3溶液中滴入AgNO3溶液:2Ag++CO32-═Ag2CO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  3-甲基-2-乙基戊烷 3-甲基-2-乙基戊烷 | |
| B. | (CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷 | |
| C. | 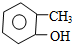 邻甲基苯酚 邻甲基苯酚 | |
| D. | 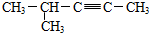 2-甲基-3-戊炔 2-甲基-3-戊炔 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com