
 �û���Ӧ��ͨʽ�ɱ�ʾΪ��ͼ��ʾ����ش��������⣺
�û���Ӧ��ͨʽ�ɱ�ʾΪ��ͼ��ʾ����ش��������⣺���� ��1������Ϊ����ɫ���壬ӦΪCl2����������ʹ������Һ����ɫ������ΪI2���÷�Ӧ������������KI�ķ�Ӧ��
��2��Al�����������������Ʒ�Ӧ��������������������������Һ��Ӧ��
��3������Ϊ����������ɫΪ��ɫ�����ΪNa��������BΪһ�ֳ�����ǿ��÷�Ӧ������ˮ��Ӧ��������������������
��4�����������Ǻ�ɫ�ǽ������嵥�ʣ�������B�����ʵ����²��ϣ���÷�ӦΪMg�ڶ�����̼��ȼ������MgO��̼��
��� �⣺��1������Ϊ����ɫ���壬ӦΪCl2����������ʹ������Һ����ɫ������ΪI2���÷�Ӧ������������KI�ķ�Ӧ����Ӧ���ӷ���ʽΪ��Cl2+2I-=I2+2Cl-���ʴ�Ϊ��Cl2+2I-=I2+2Cl-��
��2��Al�����������������Ʒ�Ӧ��Ӧ��������������������������Һ��Ӧ������Ӧ����������Һ��ȥ��Ӧ��������ʣ������������ɵ�Al2O3���ʴ�Ϊ������������Һ��
��3������Ϊ����������ɫΪ��ɫ�����ΪNa��������BΪһ�ֳ�����ǿ��÷�Ӧ������ˮ��Ӧ����������������������Ӧ����ʽΪ��2Na+2H2O=2NaOH+H2�����ʴ�Ϊ��2Na+2H2O=2NaOH+H2����
��4�����������Ǻ�ɫ�ǽ������嵥�ʣ�������B�����ʵ����²��ϣ���÷�ӦΪMg�ڶ�����̼��ȼ������MgO��̼���÷�Ӧ����ʽΪ��2Mg+CO2$\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C���ʴ�Ϊ��2Mg+CO2$\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C��
���� ���⿼�������ƶϣ���Ҫѧ����������Ԫ�ػ��������ʣ��Ѷ��еȣ�ע�����ȷ�Ӧ��þ�ڶ�����̼�е�ȼ�գ������ƶ��о������飮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ۢ٢ڢ� | C�� | �ܢڢ٢� | D�� | �ڢۢ٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʵ�ʵ��ʽ���������ʽ | |
| B�� | �������Բⶨ���ʵ���Է����� | |
| C�� | �����ʵĺ������ͼ���Ի�÷����к��л�ѧ��������ŵ���Ϣ | |
| D�� | �Ӻ˴Ź�������ͼ������֪���л�������м��ֲ�ͬ���͵���ԭ�Ӽ����ǵ���Ŀ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ⱥ��ʳ��ˮ��ȡ�������ռ�ȼҵ��
��ⱥ��ʳ��ˮ��ȡ�������ռ�ȼҵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ��22.4LNH3�к��еķ�������С��NA | |
| B�� | 1molFe3+��ȫˮ���������������������ӵ���ĿΪNA | |
| C�� | 1molCl2������NaOH��Һ��Ӧ��ת�Ƶĵ�����Ϊ2NA | |
| D�� | 0.1 mol/L�Ĵ�������Һ�к�CH3COOH��CH3COO- ��������Ϊ0.1 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� | 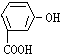 | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���ʵ���ɫ���� | B�� | ��̬�⻯����ȶ�������ǿ | ||
| C�� | ���ʵ��۵������� | D�� | ���ʵ�����������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
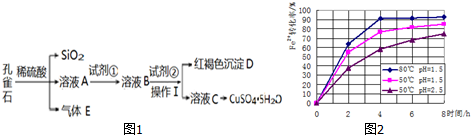
| ���� | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| ��ʼ����ʱ��pH | 2.2 | 7.6 | 4.7 |
| ��ȫ����ʱ��pH | 3.2 | 9.6 | 6.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 950 mL 111.2 g | B�� | 500 mL 117.0 g | ||
| C�� | 1000 mL 117.0 g | D�� | 1000 mL 111.2 g |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com