
【题目】(1) 把煤作为燃料可通过下列两种途径:
途径I:直接燃烧C(s)+O2(g)═CO2(g)(放热Q1kJ)
途径II:先制成水煤气:C(s)+H2O(g)═CO(g)+H2(g)(吸热Q2kJ)
再燃烧水煤气:2CO(g)+O2(g)═2CO2(g)
2H2(g)+O2(g)═2H2O(g)(共放热Q3kJ)
试回答下列问题:
①判断两种途径放出热量大小:途径I ______(填“大于”、“等于”或“小于”)途径II
②Q 1、Q 2 、Q 3 的数学关系式是________________________。
③已知1 g氢气完全燃烧生成液态水时放出热量143 kJ,18 g水蒸气变成液态水放出44 kJ的热量。
其他相关数据如下表:则表中x的值为_____________。
O===O | H—H | H—O(g) | |
1 mol化学键断裂时需要吸收的能量/kJ | 496 | 436 | x |
④简述煤通过途径Ⅱ作为燃料的意义:______________________________

(2)化学反应可视为旧键断裂和新键形成的过程。如图为白磷(P4)和P4O6分子的分子结构示意图,其他相关数据如下表所示。则反应P4 +3O2 = P4O6的热量变化为:__________________。
O===O | P—P | P—O | |
1 mol化学键断裂时需要吸收的能量/kJ | 496 | 198 | 360 |
(3)下列变化中属于放热反应的是______
A.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
B.镁条与二氧化碳反应
C.干冰升华为气体
D.碳酸钙高温锻烧
【答案】 等于 Q1 =![]() Q3 — Q2 463 燃烧充分,节约能源,污染轻 放热 1644kJ B
Q3 — Q2 463 燃烧充分,节约能源,污染轻 放热 1644kJ B
【解析】(1)①根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关,通过观察可知途径Ⅰ和途径Ⅱ是等效的,途径Ⅰ和途径Ⅱ等量的煤燃烧消耗的氧气相等,两途径最终生成物只有二氧化碳,所以途径Ⅰ放出的热量等于途径Ⅱ放出的热量;②途径I:a. C (s) + O2 (g)═CO2 (g) △H1=-Q1 kJ/mol
途径II:b. C (s)+ H2O(g)═CO (g) + H2 (g) △H2=+Q2 kJ/mol
将水煤气燃烧合并为一个热反应方程式:
c.2CO (g) + 2H2 (g) + 2O2 (g) ═ 2CO2 (g)+ 2H2O(g) △H3=-Q3 kJ/mol
根据盖斯定律,由b+![]() c可得反应a,则△H1=△H2+
c可得反应a,则△H1=△H2+![]() △H3,故有:-Q1 kJ/mol=+Q2 kJ/mol-
△H3,故有:-Q1 kJ/mol=+Q2 kJ/mol-![]() Q3 kJ/mol,则有:Q1 =
Q3 kJ/mol,则有:Q1 =![]() Q3 —Q2;③根据题意,可得热化学方程式为2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol;而18 g水蒸气变成液态水时放出44kJ热量,则2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ/mol,即-484 kJ=2×436 kJ+496 kJ-4x,解得x=463 kJ;④煤通过途径Ⅱ作为燃料的意义主要是为了提高燃料的利用率,使燃烧充分,节约能源,污染轻;(2)根据结构可知1mol白磷分子中含有6molP-P键,1molP4O6分子中有12molP-O键,P-P键能为198kJ/mol,P-O键能为360kJ/mol,O=O键能为496kJ/mol,由ΔH=反应物的总键能-生成物的总键能,故反应P4(白磷)+3O2=P4O6的反应热△H=6×198kJ/mol+3×496kJ/mol-12×360kJ/mol=-1644kJ/mol;(3)A、Ba(OH)2·8H2O晶体与NH4Cl晶体的反应属于吸热反应,选项A错误;B、镁条与二氧化碳反应是燃烧反应,属于放热反应,选项B正确;C、干冰升华为气体是吸热过程,选项C错误;D.碳酸钙高温锻烧是高温条件下的分解反应,属于吸热反应,选项D错误。答案选B。
Q3 —Q2;③根据题意,可得热化学方程式为2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol;而18 g水蒸气变成液态水时放出44kJ热量,则2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ/mol,即-484 kJ=2×436 kJ+496 kJ-4x,解得x=463 kJ;④煤通过途径Ⅱ作为燃料的意义主要是为了提高燃料的利用率,使燃烧充分,节约能源,污染轻;(2)根据结构可知1mol白磷分子中含有6molP-P键,1molP4O6分子中有12molP-O键,P-P键能为198kJ/mol,P-O键能为360kJ/mol,O=O键能为496kJ/mol,由ΔH=反应物的总键能-生成物的总键能,故反应P4(白磷)+3O2=P4O6的反应热△H=6×198kJ/mol+3×496kJ/mol-12×360kJ/mol=-1644kJ/mol;(3)A、Ba(OH)2·8H2O晶体与NH4Cl晶体的反应属于吸热反应,选项A错误;B、镁条与二氧化碳反应是燃烧反应,属于放热反应,选项B正确;C、干冰升华为气体是吸热过程,选项C错误;D.碳酸钙高温锻烧是高温条件下的分解反应,属于吸热反应,选项D错误。答案选B。


科目:高中化学 来源: 题型:
【题目】如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):

(1)电解质溶液为稀硫酸时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极上发生的反应为______________;Al电极上发生的反应为________________________________________________________________________。
(2)电解质溶液为NaOH溶液时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,Al电极上发生的反应为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g); ΔH=-49.0kJ/mol。某温度下,将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示(实线)。图中数据a(1,6)表示:在1min时H2的物质的量是6mol。
CH3OH(g)+H2O(g); ΔH=-49.0kJ/mol。某温度下,将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示(实线)。图中数据a(1,6)表示:在1min时H2的物质的量是6mol。
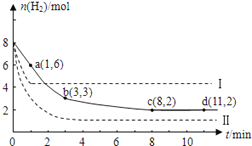
(1)第一分钟内H2的平均反应速率是________列式并计算该温度下的化学平衡常数K=______
(2)下列时间段平均反应速率最大的是_______
A.0-1min B.1-3min C.3-8min D.8-11min
(3)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线I对应的实验条件改变是__________,曲线Ⅱ对应的实验条件改变的是_____________。
(4)若在d点时向体系内充入2molCO2和2molH2O,此时V正_____V逆(大于,小于,等于)
(5)已知:
①CO(g)+1/2O2(g)=CO2(g); ΔH1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g); ΔH2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g); ΔH3=-192.2kJ/mol
在工业上常用CO和H2合成甲醇,该反应的热方程式为_____________
(6)如图是甲醇燃料电池原理示意图,回答下列问题:电池负极的电极反应是:__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
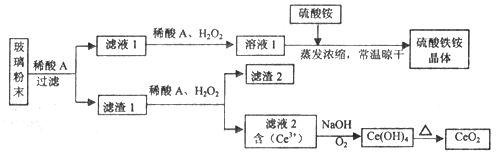
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是_____________________。
(2)滤液1中加入H2O2溶液的目的是__________________。
(3)设计实验证明滤液1中含有Fe2+_____________________。
(4)已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式____________。
(5)由滤液2生成Ce(OH)4的离子方程式__________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是___________________。
(7)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质置分数为_______(结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示。下列叙述正确的是( )

A.M的相对分子质量是180
B.1 mol M最多能与2 mol Br2发生反应
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
D.1 mol M与足量H2反应,最多消耗5 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当光束通过下列物质:①尘埃的空气 ②氢氧化钠溶液 ③蒸馏水 ④淀粉溶液,能观察到有丁达尔现象的是
A. ①② B. ②③ C. ①④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产、生活中常设计化学知识,下列说法正确的是
A. “海市蜃楼”现象是胶体的丁达尔效应造成的
B. 明矾可用于再来水的净化和消毒
C. 在香蕉箱中放入浸有KMnO4溶液的硅藻土可延长保鲜期
D. 由于碘单质受热易升华,所以炒菜时加碘盐最后放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到
蒸馏水中,所形成的分散系:①是溶液 ②是胶体 ③能产生丁达尔效应 ④分散质粒子能透过滤纸 ⑤分散质粒子不能透过滤纸 ⑥静置后,会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.①⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com