
 2NH3��g��+CO2��g��
2NH3��g��+CO2��g��| �¶ȣ��棩 | 15��0 | 20.0 | 25��0 | 30��0 | 35��0 |
| ƽ��������Ũ�ȣ���10��3 mol/L�� | 2��4 | 3��4 | 4��8 | 6.8 | 9��4 |
 NH4����OH�D ,Kb=1��8��10��5= c(NH4��)c(OH�D )/c(NH3��H2O)=c2(OH�D )/c(NH3��H2O),�ã�c(OH�D )=
NH4����OH�D ,Kb=1��8��10��5= c(NH4��)c(OH�D )/c(NH3��H2O)=c2(OH�D )/c(NH3��H2O),�ã�c(OH�D )=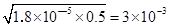 , pH=14��lg3��10-3=14-3��lg3=11.5;PH=11ʱ��c(OH�D )=10-3mol/L��c��Mg2+��=Ksp/c2(OH�D )=1��8��10��11/(10-3)2=1.8��10-5mol/L���𰸣�1.8��10-5mol/L��
, pH=14��lg3��10-3=14-3��lg3=11.5;PH=11ʱ��c(OH�D )=10-3mol/L��c��Mg2+��=Ksp/c2(OH�D )=1��8��10��11/(10-3)2=1.8��10-5mol/L���𰸣�1.8��10-5mol/L��

 ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д� Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ܱա������Ǵ�Ű�ˮ�ı�Ҫ���� |
| B��ʵ���ҳ����ű���ʳ��ˮ���ռ����� |
| C�����Ṥҵ�����У�ʹ�ù������������NH3�������� |
| D���ϳɰ���Ӧ���ýϸ��¶Ⱥ�ʹ�ô���������߰����IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����ˮ����ƽ�⣺Cl2+H2O HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz |
B����CO(g)+NO2(g) CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ���� CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ���� |
C����2NO2(g)  N2O4(g), �����¶�ƽ����ϵ��ɫ���� N2O4(g), �����¶�ƽ����ϵ��ɫ���� |
| D��SO2��������SO3�ķ�Ӧ��������������Ŀ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 HBr+HBrO����Ҫʹ��ˮ����ɫ��dz���ɲ�ȡ�Ĵ�ʩ��
HBr+HBrO����Ҫʹ��ˮ����ɫ��dz���ɲ�ȡ�Ĵ�ʩ��| A����ѹ | B������NaF���� | C��ͨ��SO2���� | D������NaI���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 PCl5��g����ƽ��ʱ��PCl5Ϊ0.40 mol�������ʱ����1.0 mol PCl3��0.50 mol Cl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ����ǣ� ��
PCl5��g����ƽ��ʱ��PCl5Ϊ0.40 mol�������ʱ����1.0 mol PCl3��0.50 mol Cl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ����ǣ� �� | A��0.40 mol | B��0.20 mol |
| C����0.20 mol | D������0.20 mol����0.40 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2B(s) + 6HBr(g) ����ȡ���������������գ�
2B(s) + 6HBr(g) ����ȡ���������������գ�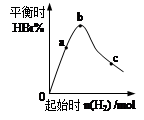
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5�������й�˵��һ����ȷ����
�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5�������й�˵��һ����ȷ����
| A��������Ӧ�ġ�H>0 |
| B��ѹǿP1>P2>P3>P4 |
| C��1100��÷�Ӧ��ƽ�ⳣ��Ϊ64mol2��L-1 |
| D��ѹǿΪP4ʱ����Y�㣺v(��)<v(��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CoCl4�� ��H��0
CoCl4�� ��H��0| A������Һ������ϵ���ȣ���Һ��ɫ���� |
| B������Һ������ϵ�ñ�ˮ���£�������Ӧ��ƽ�ⳣ����С |
| C�������£���ˮϡ�ͣ�������Ӧ��ƽ�ⳣ����С |
| D�������£���ˮϡ����һ����Χ����ҺΪ�ۺ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)��������Щ�����ٱ仯ʱ��������˵����ѧ��Ӧ�Ѵ�ƽ��״̬(�� ��)
2SO3(g)��������Щ�����ٱ仯ʱ��������˵����ѧ��Ӧ�Ѵ�ƽ��״̬(�� ��)| A�����������ܶ� | B����������ѹǿ |
| C���������������ʵ��� | D����������ƽ����Է������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com