
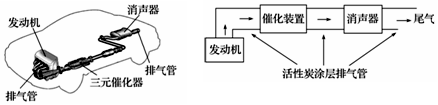
分析 (1)△H=反应物的键能总和-生成物的键能总和;
(2)根据△H-T△H<0来判断反应的自发性;
(3)A.催化剂不能改变化学平衡;
B.升高温度,正逆反应速率增大;
C.该反应为气体参与生成气体的反应,反应前后气体的质量不变,但体积数减小,结合ρ=$\frac{m}{v}$分析;
D.平衡时,其他条件不变,增大NO的浓度,反应物NO的转化率减小;
(4)A.催化剂只影响反应速率,不会改变转化率;
B.增大压强平衡向逆反应方向移动;
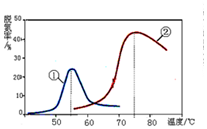
C.最高点为催化剂活性最高的温度;
D.根据图象判断,脱氨率最高的点对应的温度应是最适宜温度;
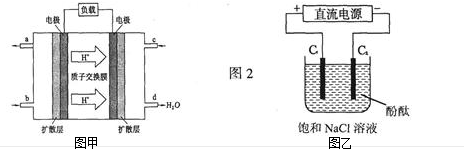
(5)①电解饱和食盐水时,反应物为氯化钠和水,生成物为氢氧化钠、氢气和氯气,据此写出反应的离子方程式;电解过程中,阳极氯离子失去生成氯气,阴极水电离的氢离子得到电子生成氢气,同时产生氢氧根离子;
②依据电极反应电子守恒计算,原电池负极电极反应CH3OH+H2O-6e-═CO2+6H+,和电解池阴极电极反应2H++2e-=H2↑存在电子守恒.
解答 解:(1)设NO中氮氧键的键能为x,
△H=反应物的键能总和-生成物的键能总和=(946+498)kJ•mol-1-2×x=180kJ•mol-1,解得x=632 kJ•mol-1,
故答案为:632;
(2)2CO(g)=2C(s)+O2(g)(△H>0、△S<0)是一个焓增、熵减的反应,任何情况下不能自发进行,所以无法消除CO的污染,
故答案为:不合理,该反应焓增、熵减,任何条件下都不能自发进行或该反应△H>0,△S<0,则△G>0;
(3)A.其他条件不变,增大催化剂与反应物的接触面积,能提高反应速率,平衡常数只与温度有关,温度不变,平衡常数不变,故A错误;
B.平衡时,其他条件不变,升高温度,逆反应速率增大,正反应速率也增大,故B错误;
C.该反应为气体参与生成气体的反应,反应前后气体的质量不变,但体积数减小,密度ρ=$\frac{m}{v}$,混合气体的密度不变时,反应达到化学平衡状态,故C正确;
D.平衡时,其他条件不变,增大NO的浓度,反应物CO的转化率增大,反应物NO的转化率减小,故D错误;
故答案为:C;
(4)A.催化剂不会影响转化率,只影响反应速率,所以第②种催化剂和第①种催化剂对转化率没有影响,故A错误;
B.反应为体积增大的反应,增大压强平衡向逆反应方向移动,脱氮率减小,故B错误.
C.图象研究的是不同催化剂在不同的温度下的活性比较,最高点为催化剂活性最大的状态,与平衡转化率无关,故C错误;
D.两种催化剂分别在55℃和75℃左右催化效率最高,说明此时催化剂的活性最大,故D正确;
故答案为:D;
(5)①电解饱和食盐水生成氢氧化钠、氢气和氯气,反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑,电解反应中,阴极水电离的氢离子得到电子生成氢气,同时产生了氢氧根离子,所以在阴极C2 (连接电源负极的电极)先变红,
故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;C2;
②原电池负极电极反应CH3OH+H2O-6e-═CO2+6H+,和电解池阴极电极反应2H++2e-=H2↑存在电子守恒,CH3OH~3H2↑~6e-,当有8g甲醇完全反应物质的量=$\frac{8g}{32g/mol}$=0.25mol,在C2上可收集到标准状况下气体的体积=0.25mol×3×22.4L/mol=16.8L,
故答案为:16.8L.
点评 本题考查了键能计算、化学平衡影响因素、电解池工作原理及其应用等知识,充分考查学生的分析、理解能力及灵活应用基础知识的能力,注意原电池和电解池工作原理中的电子守恒应用和化学平衡影响因素高频考点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | C | C. | Mg | D. | Na |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 温度/℃ | 起始时 | 平衡时 | |||
| n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
| 1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
| 2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
| 3 | b | 20.0 | 20.0 | 0 | 0 | 16.0 |
| A. | 实验1反应开始到平衡整个过程中转移的电子的物质的量为6mol | |
| B. | 实验2达平衡时,a>7.0 | |
| C. | 实验3温度b>150 | |
| D. | 实验3 CO平衡转化率比实验1小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu$\stackrel{浓硝酸}{→}$Cu(NO3)2 | B. | Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 | ||
| C. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{硝酸}{→}$Cu(NO3)2 | D. | Cu$→_{△}^{浓硫酸}$CuSO4$\stackrel{硝酸钡}{→}$Cu(NO3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com