
【题目】下列说法正确的是![]()
A.铅蓄电池放电时负极质量减轻充电时阳极质量增加
B.同温下,![]() 醋酸溶液
醋酸溶液![]() ,
,![]() 醋酸溶液
醋酸溶液![]() ,则
,则![]()
C.常温下向![]() 溶液中加入少量NaOH固体,溶液中
溶液中加入少量NaOH固体,溶液中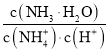 的值增大
的值增大
D.一定条件下反应![]() 当
当![]() ,则反应达到平衡
,则反应达到平衡
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某温度时,向10mL.0.1mol/LCaCl2溶液中滴加0.1mol/L的Na2CO3溶液。滴加过程中溶液中-1gc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是( )
(已知1g5=0.7)

A. x、y两点c(Ca2+)之比为2000:3 B. Ksp(CaCO3)=5×10-9
C. w点对应的分散系很稳定 D. x、y、z三点中,水的电离程度最大的为x点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①FeO投入稀H2SO4和稀HNO3中均得到浅绿色溶液
②向红砖粉末中加入盐酸,充分振荡反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液呈红色,但不一定说明红砖中含有氧化铁
③制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
④磁性氧化铁溶于稀硝酸的离子方程式为3Fe2++4H++NO![]() =3Fe3++NO↑+3H2O
=3Fe3++NO↑+3H2O
⑤氢氧化铁与HI溶液反应的离子方程式为Fe(OH)3+3H+=Fe3++3H2O
⑥Fe(OH)3不能通过Fe2O3与水反应得到,但能通过化合反应制取Fe(OH)3
⑦赤铁矿的主要成分是Fe2O3,Fe2O3为红棕色粉末
A.①③⑤B.⑥⑦C.②④⑤D.④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿原酸(见右图)是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成。下列说法正确的是( )
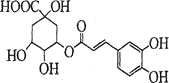
A.绿原酸的分子式为C16H20O9
B.绿原酸既能和溴水发生加成反应,又能发生取代反应
C.1 mol奎尼酸与NaOH溶液反应,最多消耗5molNaOH
D.咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
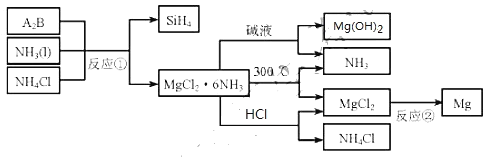
【题目】图中反应![]() 是制备
是制备![]() 的一种方法,其副产物
的一种方法,其副产物![]() 是优质的镁资源。回答下列问题:
是优质的镁资源。回答下列问题:
![]() 所含元素的简单离子半径由小到大的顺序
所含元素的简单离子半径由小到大的顺序![]() 除外
除外![]() :______。
:______。
Mg在元素周期表中的位置;______,![]() 的电子式:______。
的电子式:______。
![]() 的化学式为______,反应
的化学式为______,反应![]() 的必备条件是______。上图中可以循环使用的物质有______。
的必备条件是______。上图中可以循环使用的物质有______。
![]() 在一定条件下,由
在一定条件下,由![]() 和
和![]() 反应生成
反应生成![]() 和一种固体耐磨材料______
和一种固体耐磨材料______![]() 写化学式
写化学式![]() 。
。
![]() 为实现燃煤脱硫,向煤中加入浆状
为实现燃煤脱硫,向煤中加入浆状![]() ,使燃烧产生的
,使燃烧产生的![]() 转化为稳定的Mg化合物,写出该反应的化学方程式:______。
转化为稳定的Mg化合物,写出该反应的化学方程式:______。
![]() 用Mg制成的格氏试剂
用Mg制成的格氏试剂![]()
![]() 常用于有机合成,例如制备醇类化合物的合成路线如下:
常用于有机合成,例如制备醇类化合物的合成路线如下:
RBr![]() RMgBr
RMgBr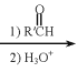
![]()
![]() :烃基;R’:烃基或
:烃基;R’:烃基或![]()
依据上述信息,写出制备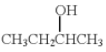 所需醛的可能结构简式:______。
所需醛的可能结构简式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N元素的单质及其化合物之间的转化关系如图所示:
![]()
回答下列问题:
(1)N元素在元素周期表中的位置为__________,画出N原子结构示意图_________。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式_____________。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可采用CO和H2合成甲醇,发生的反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0,若该反应在绝热、恒容的密闭容器中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是( )
CH3OH(g) ΔH<0,若该反应在绝热、恒容的密闭容器中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是( )
A.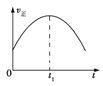
B.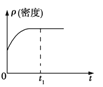
C.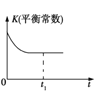
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时都会引起( )
A. CH3COOH电离程度变大 B. 溶液pH减小 C. 溶液的导电能力减弱 D. 溶液中c(H+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)作为火箭发动机的燃料,可通过反应NaClO + 2NH3 = N2H4 + NaCl + H2O制取。某化学兴趣小组尝试在实验室制取N2H4,设计了如下实验:
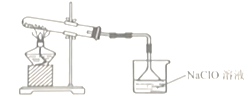
(1)制备NaClO溶液,装置如图所示。(已知:3Cl2 + 6NaOH![]() 5NaCl + NaClO3 + 3H2O)
5NaCl + NaClO3 + 3H2O)

①仪器A的名称是________________。
②连接好装置,装药品之前,必须进行的一项操作是_________。
③圆底烧瓶内发生反应的化学方程式为_______________;当生成71g氯气时,被氧化的HCl为_________mol。试管内发生反应的离子方程式为_________。
④饱和食盐水的作用是_____________,冰水的作用是____________。
(2)将NaClO溶液倒入烧杯中,持续通入NH3制取N2H4。制取氨气的化学方程式为_______。
(3)火箭发射时用N2H4作燃料,用N2O4助燃,燃烧生成两种可参与大气循环的物质。写出该反应的化学方程式______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com