
| A. | 绿色植物的光合作用是把热能转化为化学能的过程 | |
| B. | 生物能是与化学反应无关的一种能源 | |
| C. | 化学能只能以热能的形式释放 | |
| D. | 葡萄糖在人体内的氧化是放热反应 |
分析 A.绿色植物的光合作用涉及太阳能与化学能的转换;
B.生物质能以原始状态或经加工转化之后,取来作为能源;
C.化学能可转化为热能、电能等;
D.葡萄糖可为人体提供能量.
解答 解:A.绿色植物的光合作用是把太阳能转化为化学能的过程,故A错误;
B.生物质能以原始状态或经加工转化之后,取来作为能源,涉及化学反应,故B错误;
C.化学能可转化为热能、电能等,如原电池等,另外物质的燃烧还发光等,故C错误;
D.葡萄糖可为人体提供能量,可说明葡萄糖在人体内的氧化是放热反应,故D正确.
故选D.
点评 本题考查化学反应与能量变化,为高频考点,侧重考查学生的分析能力和双基的掌握,有利于培养学生良好的科学素养,难度不大,注意相关基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ①②⑤ | C. | ②③④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
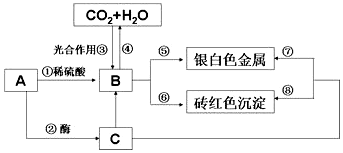
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
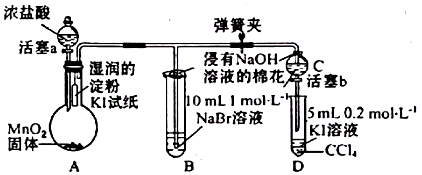
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
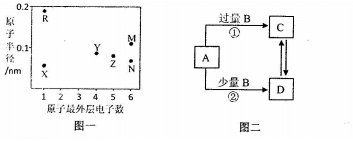
 .
. ,它能与双氧水在酸性条件下反应,生成两种无毒气体,其离子方程式为2CN-+5H2O2+2H+═N2↑+2CO2↑+6H2O.
,它能与双氧水在酸性条件下反应,生成两种无毒气体,其离子方程式为2CN-+5H2O2+2H+═N2↑+2CO2↑+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
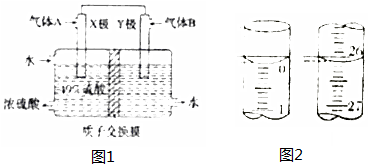
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com