
”¾ĢāÄæ”æĀĮØCæÕĘųČ¼ĮĻµē³Ų¾ßÓŠŌĮĻŅ׵Ɣ¢ÄÜĮæĆܶČøßµČÓÅµć£¬×°ÖĆČēĶ¼ĖłŹ¾£¬µē³ŲµÄµē½āÖŹČÜŅŗĪŖKOHČÜŅŗ”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©

A. ²ÉÓƶąæ×µē¼«µÄÄæµÄŹĒĢįøßµē¼«Óėµē½āÖŹČÜŅŗµÄ½Ó“„Ć껿£¬²¢ÓŠĄūÓŚŃõĘųĄ©É¢ÖĮµē¼«±ķĆę
B. ³äµēŹ±£¬µē½āÖŹČÜŅŗÖŠc(OH-)Öš½„¼õŠ”
C. ·Åµē¹ż³ĢµÄøŗ¼«·“Ó¦Ź½£ŗAl+4OH--3eØC=[Al(OH)4]-
D. ·ÅµēŹ±£¬ÓŠ4mol OH-ĶعżŅõĄė×Ó½»»»Ä¤£¬ĻūŗÄŃõĘų22.4L£Ø±ź×¼×“æö£©
”¾“š°ø”æB
”¾½āĪö”æA£®·“Ó¦Īļ½Ó“„Ć껿Ō½“󣬷“Ó¦ĖŁĀŹŌ½æģ£¬ĖłŅŌ²ÉÓƶąæ×µē¼«µÄÄæµÄŹĒĢįøßµē¼«Óėµē½āÖŹČÜŅŗµÄ½Ó“„Ć껿£¬²¢ÓŠĄūÓŚŃõĘųĄ©É¢ÖĮµē¼«±ķĆę£¬“Ó¶ųĢįøß·“Ó¦ĖŁĀŹ£¬Ń”ĻīAÕżČ·£»B”¢³äµēŹ±£¬ ×Ü·“Ó¦·½³ĢŹ½ĪŖ4[Al(OH)4]- ![]() 4Al+3O2”ü+4OH-+6H2O£¬ĖłŅŌµē½āÖŹČÜŅŗÖŠc(OH-)Öš½„Ōö“ó£¬Ń”ĻīB²»ÕżČ·£»C”¢ŌŚ¼īŠŌĢõ¼žĻĀøŗ¼«ĀĮŹ§µē×ÓÉś³ÉĀĮĄė×Ó½«ÓėĒāŃõøłĄė×Ó½įŗĻÉś³É[Al(OH)4]-£¬Ń”ĻīCÕżČ·£»D”¢O2~~~~~4e-£¬¹Ź·ÅµēŹ±£¬ÓŠ4mol OH-ĶعżŅõĄė×Ó½»»»Ä¤£¬ĻūŗÄ1molŃõĘų£¬¼“22.4L£Ø±ź×¼×“æö£©£¬Ń”ĻīDÕżČ·”£“š°øŃ”B”£
4Al+3O2”ü+4OH-+6H2O£¬ĖłŅŌµē½āÖŹČÜŅŗÖŠc(OH-)Öš½„Ōö“ó£¬Ń”ĻīB²»ÕżČ·£»C”¢ŌŚ¼īŠŌĢõ¼žĻĀøŗ¼«ĀĮŹ§µē×ÓÉś³ÉĀĮĄė×Ó½«ÓėĒāŃõøłĄė×Ó½įŗĻÉś³É[Al(OH)4]-£¬Ń”ĻīCÕżČ·£»D”¢O2~~~~~4e-£¬¹Ź·ÅµēŹ±£¬ÓŠ4mol OH-ĶعżŅõĄė×Ó½»»»Ä¤£¬ĻūŗÄ1molŃõĘų£¬¼“22.4L£Ø±ź×¼×“æö£©£¬Ń”ĻīDÕżČ·”£“š°øŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö×ÓŹ½ĪŖC6H10O4µÄÓŠ»śĪļŌŚĖįŠŌĢõ¼žĻĀĖ®½āÉś³ÉŅ»ÖÖĖįŗĶŅ»ÖÖ“¼£¬ĒŅĖįŗĶ“¼µÄĪļÖŹµÄĮæÖ®±ČĪŖ2:1.Ōņ·ūŗĻøĆĢõ¼žµÄÓŠ»śĪļÓŠ(²»æ¼ĀĒĮ¢ĢåŅģ¹¹)
A. 5ÖÖ B. 7ÖÖ C. 9ÖÖ D. 11ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń”¢Ä³Š£ŠĖȤŠ”×éµÄĶ¬Ń§½ųŠŠ”°±Č½Ļ¹żŃõ»ÆĒāŌŚ²»Ķ¬Ģõ¼žĻĀµÄ·Ö½ā”±µÄŹµŃ飬ĖūĆĒ¶ŌŹµŃéµÄ“¦ĄķČēĻĀ±ķĖłŹ¾£ŗ
ŹŌ¹Ü ×鱚 | ŹµŃ铦Ąķ | ||
¼ÓČėĢå»ż·ÖŹżĪŖ3%µÄH2O2ČÜŅŗ£ØmL£© | ĪĀ¶Č | ¼ÓČėŹŌ¼Į | |
ŹŌ¹Ü1 | 2 | ³£ĪĀ | 2µĪÕōĮóĖ® |
ŹŌ¹Ü2 | a | 90”ę | 2µĪÕōĮóĖ® |
ŹŌ¹Ü3 | 2 | ³£ĪĀ | 2µĪÖŹĮæ·ÖŹżĪŖ3.5%µÄFeCl3ČÜŅŗ |
ŹŌ¹Ü4 | 2 | b | 2µĪÖŹĮæ·ÖŹżĪŖ20%µÄøĪŌąŃŠÄ„Ņŗ |
£Ø1£©±ķøńÖŠµÄa”¢bÓ¦ĢīŠ“µÄÄŚČŻ·Ö±šŹĒ ŗĶ ”£ŌŚÉĻ±ķµÄŹµŃ铦ĄķÖŠ£¬ŃŠ¾æĮĖÄÄŠ©×Ō±äĮæ? ”£
£Ø2£©±ķÖŠµÄÄÄĮ½×éŹŌ¹Ü¶ŌÕÕ£¬æÉŃŠ¾æÉśĪļ“߻ƼĮÓėĪŽ»ś“߻ƼĮ“߻Ɗ§ĀŹµÄ²ī±š£æ ”£
£Ø3£©ŌŚĢ½¾æĪĀ¶Č¶ŌĆø»īŠŌµÄÓ°ĻģŹ±£¬ £ØĢī”°ÄÜ”±»ņ”°²»ÄÜ”±£©ÓĆ¹żŃõ»ÆĒāĪŖŹµŃé²ÄĮĻ”£
¢ņ”¢Ä³Š£ŠĖȤŠ”×éµÄĶ¬Ń§½ųŠŠĮĖ”°Ģ½¾æ½ĶÄø¾śĻø°ūŗōĪüµÄ·½Ź½”±µÄŹµŃ锣Ēė¾ŻĢā·ÖĪö×÷“š£ŗ
ĻÖĢį¹©ČōøÉĢ×£ØĆæĢ×¾łÓŠŹżøö£©ŹµŃé×°ÖĆČēĶ¼¢ń£Øa”«d£©ĖłŹ¾£ŗ

£Ø1£©ČōŅŖĢ½¾æµÄ¾ßĢåĪŹĢāŹĒ£ŗ½ĶÄø¾śŹĒ·ńŌŚÓŠŃõ”¢ĪŽŃõĢõ¼žĻĀ¾łÄܲśÉśCO2”£øł¾ŻŹµŃéÄæµÄŃ”Ōń×°ÖĆŠņŗÅ£¬ÓŠŃõĢõ¼žĻĀµÄ×°ÖĆŠņŗÅĪŖc”śb”śa”śb£¬ŌņĪŽŃõĢõ¼žĻĀµÄ×°ÖĆŠņŗÅĪŖ£ŗ £ØÓĆ×ÖÄøŗĶ¼żĶ·±ķŹ¾£©”£
£Ø2£©×°ÖĆÖŠcĘæµÄ×÷ÓĆŹĒ£ŗ £¬bĘæÖŠ³ĪĒåµÄŹÆ»ŅĖ®»¹æÉÓĆäå÷źĻć²Ż·ÓĄ¶Ė®ČÜŅŗ“śĢę£¬ŌņŃÕÉ«±ä»ÆĪŖ£ŗ ”£
£Ø3£©ĄūÓĆĶ¼¢ņĖłŹ¾×°ÖĆ£ØĻšĘ¤ČūÉĻµÄĶä¹ÜĪŖ“ųÓŠŗģÉ«ŅŗµĪµÄæĢ¶Č²£Į§¹Ü£©£¬Ģ½¾æ½ĶÄø¾śµÄĻø°ūŗōĪüĄąŠĶ”£ĻėµĆµ½ŹµŃé½įĀŪ»¹±ŲŠėĶ¬Ź±ÉčÖƶŌÕÕŹµŃ飬¶ŌÕÕŹµŃé×°ÖĆ£Ø¼ŁÉčøĆ×°ÖƱąŗÅĪŖ¢ó£©³żÓƵČĮæĒåĖ®“śĢęNaOHČÜŅŗĶā£¬ĘäĖūÉč¼ĘÓė×°ÖĆ¢ņĻąĶ¬”£
ĒėŌ¤²āÓė½įĀŪĻą·ūŗĻµÄĻÖĻ󣬲¢ĢīŠ“ĻĀ±ķ£ŗ
ŠņŗÅ | ×°ÖĆÖŠŗģÉ«ŅŗµĪµÄŅʶÆĻÖĻó | ½įĀŪ | |
×°ÖĆ¢ņ | ×°ÖĆ¢ó | ||
1 | Ļņ×óŅĘ | ²»ŅĘ¶Æ | Ö»½ųŠŠÓŠŃõŗōĪü |
2 | ²»ŅĘ¶Æ | ĻņÓŅŅĘ |
|
3 | Ļņ×óŅĘ |
| ¼Č½ųŠŠÓŠŃõŗōĪü£¬ÓÖ½ųŠŠĪŽŃõŗōĪü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×éѧɜ¶ŌĖÜĮĻ·¹ŗŠ·ĻĘśĪļµÄĖ®½āŅŗ½ųŠŠµēÉųĪö“¦Ąķ£¬Ķ¬Ź±µĆµ½¶Ō±½¶ž¼×Ėį”£ŌĄķČēĶ¼ĖłŹ¾£ØH2A±ķŹ¾¶Ō±½¶ž¼×Ėį£¬A2-±ķŹ¾¶Ō±½¶ž¼×ĖįøłĄė×Ó£©£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. µē¼«aĪŖŅõ¼«£¬µē¼«b²śÉśŃõĘų
B. ĶصēŅ»¶ĪŹ±¼äŗó£¬ĮņĖįČÜŅŗpHÉżøß
C. A2-ĶعżŅõĄė×Ó½»»»Ä¤½ųČėÅØĖõŹŅ
D. ¶Ō200mlµÄ8.3g/L¶Ō±½¶ž¼×ĖįČÜŅŗ£¬ĶصēŅ»¶ĪŹ±¼äŗó£¬ÅضČÉĻÉżµ½0.1mol/L£¬Ņõ¼«²śÉśĘųĢåĢå»ż4.48L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÕĘĪÕŅĒĘ÷Ćū³Ę”¢×é×°¼°Ź¹ÓĆ·½·ØŹĒ֊ѧ»ÆѧŹµŃéµÄ»ł“”£¬ĻĀĶ¼ĪŖČżĢ׏µŃé×°ÖĆ”£
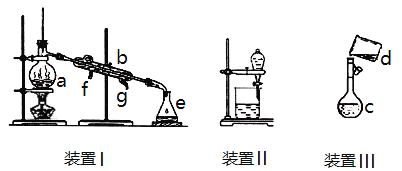
(1)Š“³öĻĀĮŠŅĒĘ÷µÄĆū³Ę£ŗa.___________________b.____________________”£
(2)ČōĄūÓĆ×°ÖĆI·ÖĄėĖÄĀČ»ÆĢ¼ŗĶ¾Ę¾«µÄ»ģŗĻĪļ£¬ĄäÄżĖ®ÓÉ_____(Ģīf»ņg)æŚĶØČė”£
(3)ÓĆ×°ÖĆII·ÖĄė»ģŗĻĪļŹ±£¬ĪŖŹ¹ŅŗĢåĖ³ĄūĮ÷ĻĀ£¬Ó¦½ųŠŠµÄ²Ł×÷ŹĒ_____________”£
(4)ŹµŃéŹŅÓĆNa2CO3”¤10H2O¾§ĢåÅäÖĘ0.05mol/LµÄNa2CO3ČÜŅŗ970mL”£
¢ŁÓ¦ÓĆĶŠÅĢĢģĘ½³ĘČ”Na2CO3”¤10H2OµÄÖŹĮæŹĒ_____________g”£
¢Ś×°ÖĆIIIŹĒijĶ¬Ń§×ŖŅĘČÜŅŗµÄŹ¾ŅāĶ¼”£Ķ¼ÖŠµÄ“ķĪóŹĒ___________________”£
(5)¶ØČŻŹ±£¬ø©ŹÓæĢ¶ČĻߣ¬¶ŌĖłÅäČÜŅŗÅØ¶ČµÄÓ°Ļģ£ŗ_____________(Ģī£ŗĘ«“ó”¢Ę«Š””¢»ņĪŽÓ°Ļģ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĆܱÕČŻĘ÷ÖŠ£¬Ņ»¶ØĮæ»ģŗĻĘųĢå·¢ÉśĻĀĮŠ·“Ó¦£ŗ aM£Øg£©£« bN£Øg£©![]() cW(g)£¬“ļŅ»Ę½ŗāŗ󣬲āµĆMĘųĢåµÄÅضČĪŖ0.5mol/L”£µ±ŌŚŗćĪĀĻĀ£¬½«ĆܱÕČŻĘ÷µÄĢå»żĄ©“ó1±¶£¬ŌŁ“ļĘ½ŗāŹ±£¬²āµĆMĘųĢåµÄÅضČĪŖ0.3mol£ÆL”£ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
cW(g)£¬“ļŅ»Ę½ŗāŗ󣬲āµĆMĘųĢåµÄÅضČĪŖ0.5mol/L”£µ±ŌŚŗćĪĀĻĀ£¬½«ĆܱÕČŻĘ÷µÄĢå»żĄ©“ó1±¶£¬ŌŁ“ļĘ½ŗāŹ±£¬²āµĆMĘųĢåµÄÅضČĪŖ0.3mol£ÆL”£ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. ·“Ó¦ĖŁĀŹŌö“ó B. Ę½ŗāĻņÓŅŅʶÆ
C. NµÄ×Ŗ»ÆĀŹĢįøß D. WµÄĢå»ż·ÖŹż½µµĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĶ¬·ÖŅģ¹¹ĢåŹżÄæµÄŠšŹöÖŠ£¬ÕżČ·µÄŹĒ
A. C2H6OÖ»ÓŠŅ»ÖÖ½į¹¹
B. ·Ö×ÓŹ½·ūŗĻC5H11Cl µÄ»ÆŗĻĪļÓŠ6ÖÖ
C. ŅŃÖŖ¶žĀȱ½ÓŠ3ÖÖĶ¬·ÖŅģ¹¹Ģ壬ŌņĖÄĀȱ½µÄĶ¬·ÖŅģ¹¹ĢåµÄŹżÄæĪŖ3ÖÖ
D. ·ĘµÄ½į¹¹¼ņŹ½ĪŖ![]() £¬ĖüÓėĻõĖį·“Ó¦£¬æÉÉś³É10ÖÖŅ»Ļõ»łČ”“śĪļ
£¬ĖüÓėĻõĖį·“Ó¦£¬æÉÉś³É10ÖÖŅ»Ļõ»łČ”“śĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬¶žŌŖČõĖį H2Y ČÜŅŗÖŠµĪ¼Ó KOH ČÜŅŗ£¬ĖłµĆ»ģŗĻČÜŅŗµÄ pH ÓėĄė×ÓÅØ¶Č±ä»ÆµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ

A. ĒśĻß M ±ķŹ¾ pHÓė lg![]() µÄ±ä»Æ¹ŲĻµ
µÄ±ä»Æ¹ŲĻµ
B. aµćČÜŅŗÖŠ£ŗc(H+) ØD c(OH-)£½2c(Y2£)£«c(HY-) ØD c(K+)
C. H2Y µÄµŚ¶ž¼¶µēĄė³£ŹżKa2(H2Y)£½10£4.3
D. ½»µćbµÄČÜŅŗÖŠ£ŗc(H2Y)£½c(Y2-)£¾c(HY-)£¾c(H+)£¾c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
A. 1 mol NH3Ėłŗ¬ÓŠµÄŌ×ÓŹżĪŖNA
B. ½«100 mL 0.1 mol”¤L-1µÄFeCl3ČÜŅŗµĪČė·ŠĖ®ÖŠæÉÖʵĆFe(OH)3½ŗĮ£µÄŹżÄæĪŖ0.01NA
C. ³£ĪĀ³£Ń¹ĻĀ£¬48gO2ŗĶO3µÄ»ģŗĶĪļÖŠĖłŗ¬ŃõŌ×ÓŹżĪŖ3NA
D. 1L 0.1 mol”¤L-1 NaClČÜŅŗÖŠĖłŗ¬µÄNa+ĪŖNA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com