
| A、混合气体的压强 |
| B、C的体积分数 |
| C、混合气体的密度 |
| D、混合气体的平均相对分子质量 |
| 总质量 |
| 体积 |
| 总质量 |
| 总物质的量 |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
| 组号 | 反应温度 (℃) | 参加反应的物质 | 体积(mL) | |||
| Na2S2O3 | H2SO4 | |||||
| 体积(mL) | 浓度( mol?L-1 ) | 体积(mL) | 浓度( mol?L-1) | |||
| A | 10 | 5 | 0.1 | 10 | 0.1 | 15 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 20 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 20 |
| D | 30 | 10 | 0.08 | 15 | 0.08 | 5 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
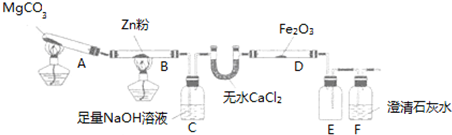
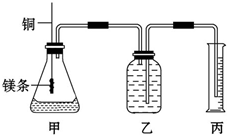 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Na+、HCO3-、Cl- |
| B、Cu2+、Na+、Cl-、SO42- |
| C、Mg2+、K+、SO42-、OH- |
| D、Ag+、Al3+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:

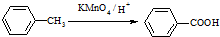
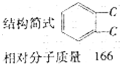
 (苯胺,易被氧化)
(苯胺,易被氧化)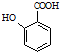 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物有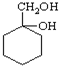 最合理的方案(不超过4步)
最合理的方案(不超过4步) .
.查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀硫酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加少量酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 酸性KMnO4溶液褪色 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室中某试剂瓶的标签严重破损,只能隐约看到如图所示部分:
实验室中某试剂瓶的标签严重破损,只能隐约看到如图所示部分: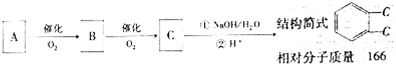
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com