��1��ijһ��Ӧ��ϵ���з�Ӧ��������ﹲ5�����ʣ�S��H
2S��HNO
3��NO��H
2O��д���÷�Ӧ�Ļ�ѧ����ʽ����ƽ
������Ӧ������ת����0.3mol���ӣ������������������
g��
��2��ͬһ���ʳ���̬����ֵ���Һ̬����ֵ��֮����̬����ֵ��С����ͬ��ͬѹ��һ����ѧ��Ӧ�����������������ڷ�Ӧ�����������Ϳ��Դ�����Ϊ�÷�Ӧ���ر�Ϊ0��ij��ѧ��ȤС�飬ר���о�������Ԫ�ؼ���ijЩ������IJ������ʣ������������£�
a���ڣ�Te��Ϊ���壬H
2TeΪ���壬Te��H
2����ֱ�ӻ��ϳ�H
2Te
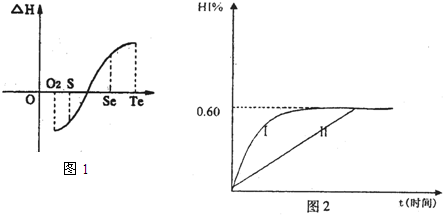
b�������ʵ�������������������H
2��Ӧ���ʱ������ͼ1��ʾ��
��ش��������⣺
H
2���ϵķ�Ӧ
��������ų��������ա�����������Ŀ������Ϣ�������ΪʲôTe��H
2����ֱ�ӻ���
��
��3���ڸ��ӵķ�Ӧ�У�Ҫ���Ƿ�Ӧ���Ⱥ�˳����֪
N+
Al+2H
2O�TAl��OH��
3��+NH
3?H
2O�����е����ʵ�����
N��Al
3+��H
+�����Һ�У������μ�NaOH��Һ��ֱ�������������Ͻ��裬���η������������ӷ�Ӧ�����У�
�ڶ������ӷ�Ӧ�����ӷ���ʽ��
��
���һ�����ӷ�Ӧ�����ӷ���ʽ��
��
��4����1mol I
2��g����2mol H
2��g������ij2L�ܱ������У���һ���¶��·�����Ӧ��
H
2��g��+I
2��g��?2HI��g������H��0������ƽ�⣮HI���������HI%��ʱ�ʱ仯������ͼ2��ʾ��
�ٴﵽƽ��ʱ��I
2��g�������ʵ���Ũ��Ϊ
mol/L��
�ڱ��ּ���ķ�Ӧ������ʵ������䣬���ı䷴Ӧ��������ijһ������HI%�ı仯������1��ʾ��������������ǣ�д�����еĿ����ԣ�
�����������£�ƽ�ⳣ��Kֵ
�����������С���������䡱���ܱ��Ҳ���ܱ�С����
���������¶Ȳ��䣬����һ��ͬ��2L�ܱ������м���1mol H
2��g����2mol HI��g����������Ӧ�ﵽƽ��ʱ��H
2���������Ϊ
��




