
| A. | 简单离子半径:W<X<Z | |
| B. | W与X形成的化合物溶于水后溶液呈碱性 | |
| C. | 气态氢化物的热稳定性:W<Y | |
| D. | 最高价氧化物的水化物的酸性:Y>Z |
分析 四种短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X是钠;Z与X形成的离子化合物的水溶液呈中性,说明这种盐不水解,Z只能是第三周期的非金属元素,且Z的氢化物的水溶液属于强酸,则Z是氯;W、X的简单离子具有相同电子层结构,则W在第二周期且是非金属元素,可能是氮和氧;W与Y同族,
Y在X与Z之间,位置关系如图: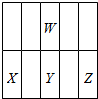 ,据此解答.
,据此解答.
解答 解:四种短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X是钠;Z与X形成的离子化合物的水溶液呈中性,说明这种盐不水解,Z只能是第三周期的非金属元素,且Z的氢化物的水溶液属于强酸,则Z是氯;W、X的简单离子具有相同电子层结构,则W在第二周期且是非金属元素,可能是氮和氧;W与Y同族,
Y在X与Z之间,位置关系如图: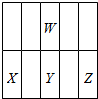 ,
,
A.X、W离子的电子层为2层,Z离子即氯离子电子层为3层,电子层多半径大,电子层结构相同时,序小半径反而大,
则简单离子半径大小顺序是:X<W<Z,故A错误;
B.W在第二周期且是非金属元素,可能是氮和氧,与钠形成的化合物可能是氮化钠,氧化钠,过氧化钠,它们与水反应都能生成氢氧化钠使溶液呈碱性,故B正确;
C.W与Y处于同于主族,从上到下,非金属性逐渐减弱,气态氢化物的热稳定性逐渐减弱,则W>Y,故C错误;
D.Y与Z处于同同期,从左到右,非金属性逐渐增强,最高价氧化物的水化物的酸性逐渐增强,则Z>Y,故D错误;
故选:B.
点评 本题考查了原子结构与元素周期表的关系,正确推断各元素为解答关键,在答题时,画出各元素的位置关系使解题更快也更准确,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
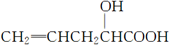 在不同条件下至少可能发生7种不同类型的反应:
在不同条件下至少可能发生7种不同类型的反应:| A. | ②④⑥⑦ | B. | ①③⑤⑥ | C. | ②③④⑤ | D. | ①③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丁烷也称异丁烷 | B. | 由乙烯生成乙醇属于加成反应 | ||
| C. | C4H9Cl有3种同分异构体 | D. | 油脂和蛋白质都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
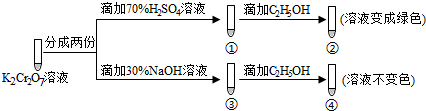
| A. | ①中溶液橙色加深,③中溶液变黄 | |
| B. | ②中Cr2O72-被C2H5OH还原 | |
| C. | 对比②和④可知K2Cr2O7酸性溶液氧化性强 | |
| D. | 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一阶段中阴、阳两极产生的气体混合引燃后,恰好完全反应得到HCl | |
| B. | 阴极自始至终只产生H2 | |
| C. | 电解过程中,溶液的pH不断增大,最后等于7 | |
| D. | 电解过程中,Na+和SO42-的物质的量保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol•L-1 CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 将CH3COONa溶液从20℃升温至30℃,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| C. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(C{l}^{-})}$>1 | |
| D. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com