
【题目】已知对于电离常数为Ka的某一元弱酸滴定过程中,pH突变随其浓度的增大而增大,且浓度主要影响滴定终点和滴定终点之后的曲线部分。常温下,用不同浓度的NaOH溶液分别滴定20 mL与其同浓度的某弱酸HA溶液,滴定曲线如图所示。下列说法不正确的是( )
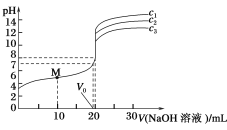
A.由图可知,c1>c2>c3
B.M点溶液中存在:c(H+)+c(HA)=c(OH-)+c(A-)
C.恰好中和时,溶液中离子浓度的大小关系:c(Na+)>c(A-)>c(OH-)>c(H+)
D.由pH=7的溶液计算得:Ka=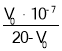 (V0是消耗的NaOH溶液的体积)
(V0是消耗的NaOH溶液的体积)
【答案】B
【解析】
A.NaOH浓度越大,溶液pH越大;
B.M点为加入NaOH体积为10mL,此时恰好生成起始时等量的NaA和HA,根据电荷守恒分析;
C.恰好中和时,溶液中恰好生成NaA,溶液呈碱性,A水解;
D.溶液中pH=7时,c(H+)=c(OH),根据电荷守恒和物料守恒计算;
A.NaOH浓度越大,溶液pH越大,根据图象,滴定终点之后溶液pH顺序大小为:c1>c2>c3,所以浓度大小为c1>c2>c3,故A正确;
B.M点为加入NaOH体积为10mL,此时恰好生成起始时等量的NaA和HA,根据电荷守恒:c(Na+)+c(H+)=c(OH)+c(A),故B错误;
C.恰好中和时,溶液中恰好生成NaA,溶液呈碱性,A水解,溶液中离子浓度大小关系为:c(Na+)>c(A)>c(OH)>(H+),故C正确;
D.溶液中pH=7时,c(H+)=c(OH),根据电荷守恒:c(Na+)+c(H+)=c(OH)+c(A),则有c(Na+)=c(A),此时消耗NaOH溶液体积为V0,所以![]() ,根据物料守恒:
,根据物料守恒:![]() ,则
,则![]() ,所以
,所以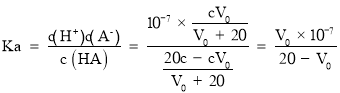 ,故D正确;
,故D正确;
故答案选:B。


科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
A.至少存在3种离子
B.Cl-一定存在,且c(Cl)≥0.4mol/L
C.SO42-、NH4+、一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li、Fe、As均为重要的合金材料,NA为阿伏加德罗常数的值。回答下列问题:
(1)基态Li原子核外电子占据的空间运动状态有________个,占据最高能层电子的电子云轮廓图形状为_________。
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为_________。
(3)基态Fe3+比基态Fe2+稳定的原因为____________。
(4)KSCN和K4[Fe(CN)6]均可用于检验Fe3+。
①SCN-的立体构型为_______,碳原子的杂化方式为_____________。
②K4[Fe(CN)6]中所含元素的第一电离能由大到小的顺序为__________(用元素符号表示);1 mol [Fe(CN)6]4-中含有σ键的数目为____________。
(5)H3AsO3的酸性弱于H3AsO4的原因为____________________。
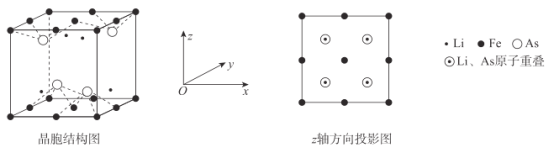
(6)Li、Fe和As可组成一种新型材料,其立方晶胞结构如图所示。若晶胞参数为a nm,阿伏加德罗常数的值为NA,则该晶体的密度可表示为______g●cm-3。(列式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷、硫、氯、砷等是农药中的重要组成元素。回答下列问题:
(1)基态砷原子的核外价电子排布式为_______________ 。
(2)生产农药的原料 PSCl3 中 P、S、Cl 的第一电离能由大到小的顺序为____电负性由大到小的顺序为__________________________。
(3)H2SO4为粘稠状 难挥发性的酸 ,而 HNO3 是易挥发的酸,其原因是__________
(4)COS(羰基硫)可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为________,所含共价 键的类型为_____________,N2O与CO2互为等电子体 ,且N2O 分子中O只与一个N相连,则N2O的电子式为_______________ 。
(5)AlP 因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。

①磷化铝的晶体类型为 _____________________ 。
②A、B 点的原子坐标如图所示,则C点的原子坐标为 __________________ 。
③磷化铝的晶胞参数a = 546.35 pm(l pm=10—12 m), 其密度为________g/cm3( 列出计算式即可,用NA表示阿伏加德罗常数的数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为 45.3g 的该结晶水合物,分别制成溶液向其中一份逐滴加入 NaOH 溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出, 该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到 2.24L 该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入 Ba(OH)2 溶液,开始现象类似,但最终仍有白色沉淀; 过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体 46.6g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是_____和_____,阴离子是_____;
(2)试通过计算确定该结晶水合物的化学式。写出计算过程:_____假设过程中向该溶液中加入的 Ba(OH)2 溶液的物质的量浓度为 2.0molL1 。
(3)加入_____mLBa(OH)2 溶液时,所得沉淀的总物质的量最大。
(4)请在如图中画出生成沉淀的物质的量与加入 Ba(OH)2 溶液体积的关系示意图_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.10 mol·L-1的Na2CO3溶液中逐滴加入稀盐酸,加入的HCl与原溶液中Na2CO3的物质的量之比f[f=![]() ]与混合液pH的关系如图所示。下列说法正确的是( )
]与混合液pH的关系如图所示。下列说法正确的是( )

A.f=0时,溶液中:c(Na+)=2c(![]() )
)
B.f=0.5时,溶液中:c(![]() )>c(
)>c(![]() )
)
C.f=1时,溶液中:c(Na+)+c(H+)=2c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
D.f=2时,溶液中:![]() c(Na+)=c(
c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用硫酸酸化的CrO3遇到酒精后,其颜色会从红色变为蓝绿色,人们利用这一反应可以判断司机是否酒后驾车,反应的方程式为:CrO3+C2H5OH+H2SO4→Cr2(SO4)3+CH3CHO+H2O
(1)配平上述反应方程式_____。
(2)该反应中氧化剂是_____,被氧化的元素是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是

A.用水湿润的pH试纸测量某溶液的pH
B.用量筒量取20 mL0.5000 mol·L-1 H2SO4溶液于烧杯中,加水80mL,配制成0.1000 mol· L-1H2SO4溶液
C.实验室用图2所示装置制取少量氨气
D.实验室用图3所示装置除去Cl2中的少量HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)乙炔在Pd表面选择加氢的反应机理如图,其中吸附在Pd表面上的物种用*标注。

上述反应为_____(填“放热”或“吸热”)反应,历程中最小能垒(活化能)为_____kJ/mol,该步骤的化学方程式为_____。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的氮氧化物脱除技术。原理为:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) △H=﹣11.63 kJ/mol,在2 L密闭容器中,使用不同的催化剂A、B、C,产生N2的物质的量随时间变化如图所示。下列说法正确的_____。
5N2(g)+6H2O(g) △H=﹣11.63 kJ/mol,在2 L密闭容器中,使用不同的催化剂A、B、C,产生N2的物质的量随时间变化如图所示。下列说法正确的_____。

A.用催化剂A前50s平均反应速率v(N2)=2.5×10﹣2 mol/(Ls)
B.体系各物质状态不变时,反应在任何温度下均可自发进行
C.分离出体系中的H2O(g)有利于氮氧化物的脱除
D.用催化剂C达到平衡时,N2产率最小
(3)废气的变废为宝越来越成为人们共同关注的焦点,某化学课外小组查阅资料得知:
2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
Ⅰ.2NO(g)![]() N2O2(g) (快) v1正=k1正c2(NO),v1逆═k1逆c(N2O2) △H1<0
N2O2(g) (快) v1正=k1正c2(NO),v1逆═k1逆c(N2O2) △H1<0
Ⅱ.N2O2(g)+O2(g)![]() 2NO2(g)(慢) v2正=k2正c(N2O2)c(O2),v2逆=k2逆c2(NO2) △H2<0
2NO2(g)(慢) v2正=k2正c(N2O2)c(O2),v2逆=k2逆c2(NO2) △H2<0
请回答下列问题:
①一定温度下,2NO(g)+O2(g)![]() 2NO2(g)平衡常数K=_____(用k1正、k1逆、k2正、k2逆表示)。
2NO2(g)平衡常数K=_____(用k1正、k1逆、k2正、k2逆表示)。
②研究发现NO转化为NO2的反应速率随温度的升高而减慢,原因是_____。
③已知:N2O4(g)![]() 2NO2(g),N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2)。一定温度下,相应的速率与压强关系如图所示,图中能表示该反应达到平衡状态的两个点是_____,可以表示该反应正向进行的两个点是_____。
2NO2(g),N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2)。一定温度下,相应的速率与压强关系如图所示,图中能表示该反应达到平衡状态的两个点是_____,可以表示该反应正向进行的两个点是_____。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com