
【题目】“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题: 高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)Fe(s)+CO2(g)△H>0.已知在1 100℃时,该反应的化学平衡常数K=0.263.
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值(填“增大”、“减小”或“不变”);
②1100℃时测得高炉中,c(CO2)=0.025molL﹣1 , c(CO)=0.1molL﹣1 , 则在这种情况下,该反应向进行(填“左”或“右”),判断依据是 .
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】在酸性溶液中,可大量共存的离子是( )
A. K+ Na+ OH- SO42-
B. Mg2+ SO42- NH4+ Cl-
C. K+ Na+ HCO3- Cl-
D. K+ Na+ NO3- CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:aA(g)+bB(g) cC(g)+dD(g);根据图回答:
①压强 P1P2;(a+b)(c+d)(填“>”或“<”下同).
②温度t1℃t2℃;△H0.
③保持体积和温度不变,通入He,平衡会移动(填“正向”、“逆向”或“不”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得: 3SiO2(s)+6C(s)+2N2(g)═Si3N4(s)+6CO(g)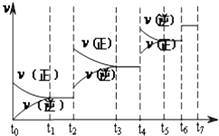
(1)该反应的平衡常数表达式为K=
(2)若知上述反应为放热反应,则其反应热△H0(填“>”、“<”或“=”);升高温度,其平衡常数值(填“增大”、“减小”或“不变”); 若已知CO生成速率为v(CO)=18molL﹣1min﹣1 , 则N2消耗速率为v(N2)=
(3)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图.图中t4时引起平衡移动的条件可能是;
(4)图中表示平衡混合物中CO的含量最高的一段时间是 .
(5)已知:2H2(g)+O2(g)═2H2O(g);△H=﹣483.6kJmol﹣1;H2O(g)=H2O(l)△H=﹣44kJmol﹣1 , ;由此可知H2燃烧热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种常见的金属单质,A元素在地壳中含量位列第6,A的密度为0.97 g/cm3;B为紫红色固体,锈蚀时变为绿色;C在空气中加热熔化但不滴落;D在氧气中燃烧,火星四射。根据以上信息回答下列问题:
(1)写出对应化学式:A________,B________,C________,D________。
(2)A在室温下与氧气反应时生成________,D在空气中锈蚀生成的氧化物为________。
(3)写出下列化学方程式:
①A在空气中燃烧_______________________________________________________;
②B长期置于空气中变为绿色物质______________________________________________。
(4)将5 g钠铝合金投入到200 mL的水中,固体完全溶解,产生4.48 L标准状况下的气体,溶液中只有一种溶质。经过分析得出钠铝合金中两种金属的物质的量之比为________,所得溶液中溶质的物质的量浓度为____________(假设溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为 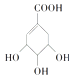 ,关于它的叙述中不正确的是( )
,关于它的叙述中不正确的是( )
A.该有机物能使溴的四氯化碳溶液褪色
B.该有机物发生消去反应可得到芳香烃
C.该有机物在一定条件下可发生氧化反应
D.1 mol该有机物最多可与1 mol NaHCO3反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为了探究SO2和氯水的漂白性,设计了如图所示实验装置。
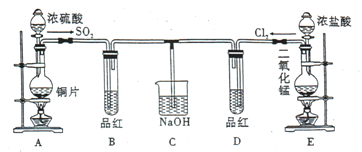
(1)写出A中反应的化学方程式:___________, 浓硫酸表现出_____性。
(2)实验室用装置E制备Cl2,离子方程式为____________。该反应中的还原剂是_______(填化学式)。
(3)①装置A和E中,常用于萃取操作的仪器是__________(填名称)。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B.______,D._____。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入品红溶液中,结果发现品红溶液未褪色,并且生成了两种常见的强酸,请你分析该现象的原因:__________(用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com