
| A.SO2、SO3、O2的体积分数相等 |
| B.单位时间内生成amolO2的同时生成amolSO3 |
| C.单位时间内消耗amolO2的同时消耗2amolSO2 |
| D.反应若在容积固定的密闭容器中进行,温度一定时,反应混合物的总压强不随时间变化 |
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题
| 物质的量 | CO2 | H2 | CO | H2O |
| 甲 | a mol | a mol | 0 mol | 0 mol |
| 乙 | 2a mol | a mol | 0 mol | 0 mol |
| 丙 | 0 mol | 0 mol | a mol | a mol |
| 丁 | a mol | 0 mol | a mol | a mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.容器内压强不随时间的变化而变化 |
| B.X、Y、Z、W的浓度比保持不变 |
| C.X的消耗速率与Z的生成速率相等 |
| D.c(X)?c(Y)=c(Z)?c(W) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH3的消耗速率等于NH3的生成速率 |
| B.混合气体的密度保持不变 |
| C.NO的物质的量保持不变 |
| D.NH3和O2的浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应容器内的压强不随时间改变 |
| B.反应容器内P、Q、R、S四者共存 |
| C.P的生成速率和S的生成速率相等 |
| D.反应容器内的气体总物质的量不随时间变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合气体的压强 | B.混合气体的密度 |
| C.C、D的物质的量的比值 | D.气体的总物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.①④⑥ | C.②③⑥ | D.②③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
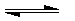 pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).
pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).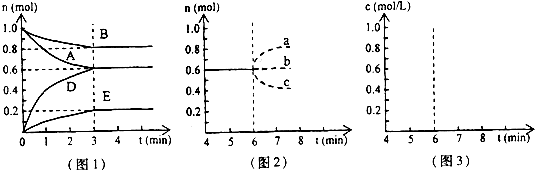
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com