【答案】
分析:A、四氯化碳中氯原子中未成键的电子对未标出;
B、氟化钠是离子化合物,由钠离子与氟离子构成;
C、硫原子得2个电子形成硫离子,根据核外电子排布规律书写判断;
D、碳-12表示质子数为6,中子数为6的碳原子.
解答:解:A、CCl
4为共价化合物,四氯化碳中碳原子和氯原子均满足8电子稳定结构,电子式为
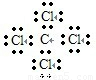
,故A错误;
B、氟化钠是离子化合物,由钠离子与氟离子构成,电子式为
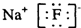
,故B正确;
C、硫原子得2个电子形成硫离子,质子数是16,核外电子数是18,硫离子的结构示图
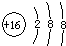
,故C正确;
D、碳-12表示质子数为6,中子数为6的碳原子,原子符号为
612C,故D正确.
故选A.
点评:本题考查化学用语的书写,难度不大,可以根据所学知识进行回答.

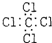
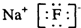
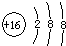
 ,故A错误;
,故A错误;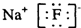 ,故B正确;
,故B正确;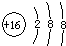 ,故C正确;
,故C正确;
