
| A. | 离子半径:Na+<S2-<Cl-<K+ | B. | 还原性:I-<Br-<-Cl<F- | ||
| C. | 稳定性:SiH4<PH3<HCl<HBr | D. | 溶解性:BaO4<CaSO4<MgSO4. |
分析 A、核外电子排布相同的离子,核电核数越大半径越小;
B、同一主族的元素,从上而下,元素的非金属性逐渐减弱,对应的阴离子的还原性越强;
C、元素的非金属性越强,则气态氢化物的稳定性越强;
D、第二主族的元素,从上到下,对应的硫酸盐的溶解度逐渐降低.
解答 解:A、粒子的电子层数越多,半径越大,故Na+的半径最小;当电子层数相同时,核电荷数越大,则半径越小,故S2->Cl->K+,故大小顺序是S2->Cl->K+>Na+,故A错误;
B、同一主族的元素,从上而下,元素的非金属性逐渐减弱,对应的阴离子的还原性越强,F、Cl、Br、I为第VIIA族的元素,故对应的阴离子的还原性为I->Br->Cl->F-,故B错误;
C、元素的非金属性越强,则气态氢化物的稳定性越强,由于非金属性Cl>Br>P>Si,故氢化物的稳定性为HCl>HBr>PH3>SiH4,故C错误;
D、第二主族的元素,从上到下,对应的硫酸盐的溶解度逐渐降低,即溶解性BaSO4<CaSO4<MgSO4,故D正确.
故选D.
点评 本题考查了元素周期表中元素性质的相似性和递变性,难度不大,掌握元素周期律是解题的关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
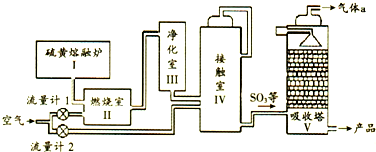
| A. | Ⅱ中主要反应的热化学方程式:S(s)+O2(g)?SO3(g)△H=-297kJ•mol-1S(s)+O2(s)=SO2(g)△H=-297kJ•mol-1 | |
| B. | Ⅳ中主要反应的化学方程式:2SO2+O2(s) $?_{△}^{催化剂}$SO3 | |
| C. | Ⅳ中使用催化剂可提高化学反应速率和平衡转化率 | |
| D. | Ⅴ中气体a 可以直接排放到大气中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCl2中既含有离子键又含有共价键 | |
| B. | Na0H中既含有离子键又含有共价键 | |
| C. | Na2O2中只含有离子键 | |
| D. | 由非金属元素组成的物质NH4Cl中只有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
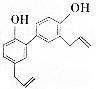 中药厚朴皮中起抗菌作用的有效成分为厚朴酚,其结构简式如图所示.该物质具有持久的肌肉松弛作用和极强的抗菌作用,临床上主要用于镇静中枢神经、抗真菌等.
中药厚朴皮中起抗菌作用的有效成分为厚朴酚,其结构简式如图所示.该物质具有持久的肌肉松弛作用和极强的抗菌作用,临床上主要用于镇静中枢神经、抗真菌等.| A. | 1个厚朴酚分子中含有16个碳原子 | |
| B. | 厚朴酚能使酸性KMnO4溶液褪色,遇FeCl3溶液显色 | |
| C. | 1mol厚朴酚与足量NaHCO3溶液反应放出22.4LCO2(标准状况) | |
| D. | 1mol厚朴酚能与4molBr2(Br2的CCl4溶液)反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去 | |
| B. | 将苯酚晶体放入少量水中,加热时全部溶解,冷却后溶液仍澄清透明 | |
| C. | 苯酚的酸性很弱,不能使指示剂变色,但可以与NaCHO3反应放出CO2 | |
| D. | 苯酚有毒,但其稀溶液可直接用作防腐剂和消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子方程式 | 评价 |
| A.亚磷酸是一种二元酸,在其中加入过量的烧碱溶液: H3PO3+3OH-=PO33-+3H2O | 正确 |
| B.在亚硫酸中加入少量的次氯酸钠溶液 H2SO3+ClO-=Cl-+2H++SO42- | 正确 |
| C.在碳酸氢镁溶液中加入过量氢氧化钠溶液: Mg2++2HCO3-+2OH-=Mg CO3↓+CO32-+2H2O | 错误:生成物应是 Mg(OH)2和Na2CO3 |
| D.在过氧化钠中加入稀硫酸: 2Na2O2+4H+=4Na++2H2O+O2↑ | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com