
 .
. .
. 分析 A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素,则A为氢元素;B的+1价阳离子和C的-1价阴离子都与氖原子具有相同的电子层排布,则B为Na元素,C为F元素;D在C的下一周期,可与B形成BD型离子化合物,则D为Cl元素;E和C为同一周期元素,其最高价氧化物的水化物为强酸,则E为N元素,据此解答.
解答 解:A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素,则A为氢元素;B的+1价阳离子和C的-1价阴离子都与氖原子具有相同的电子层排布,则B为Na元素,C为F元素;D在C的下一周期,可与B形成BD型离子化合物,则D为Cl元素;E和C为同一周期元素,其最高价氧化物的水化物为强酸,则E为N元素.
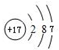
(1)D为Cl元素,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)E的最高价氧化物对应水化物与其气态氢化物反应的方程式为:HNO3+NH3=NH4NO3,故答案为:HNO3+NH3=NH4NO3;
(3)B的最高价氧化物对应的水化物为NaOH,含有离子键、共价键,故答案为:离子键、共价键;
(4)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
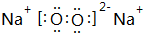
(5)B的单质在空气中点燃生成过氧化钠,电子式为 ,故答案为:
,故答案为: .
.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对化学用语与元素化合物性质的考查,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用溴水鉴别甲苯、己烷、己烯 | |
| B. | 将稀硫酸、稀硝酸和苯混合加热制硝基苯 | |
| C. | 苯和硝基苯混合物采用分液的方法分离 | |
| D. | 用CuSO4溶液除去由电石和水反应生成的乙炔气体中的杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
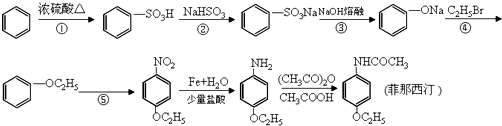
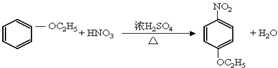 ;
;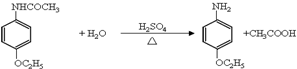 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
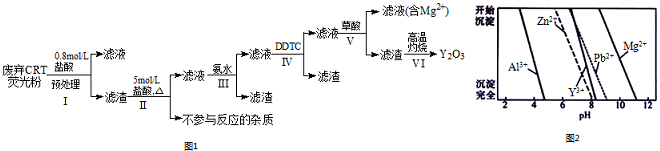
| 阶段/含量%/成分 | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验步骤 |
| A | 探究催化剂对化学反应速率的影响 | 向H2O2溶液中滴加少量FeCl3溶液 |
| B | 探究乙醇能发生氧化反应 | 将铜丝在酒精灯加热后,立即伸入无水乙醇中 |
| C | 探究石蜡油分解的产物不都是烷烃 | 将石蜡油加强热产生的气体通入溴水中 |
| D | 探究浓度对反应速率的影响 | 取少量等质量的相同铁粉,分别加入1mol/L的硫酸和18mol/L的硫酸中,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
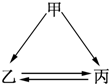 \如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
\如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  和C2H5OH 和C2H5OH | B. | 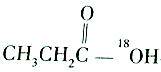 和C2H518OH 和C2H518OH | ||
| C. | 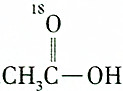 和CH3CH2CH218OH 和CH3CH2CH218OH | D. | 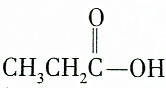 和C2H5OH 和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 C、Be、Cl、Fe等元素及其化合物有重要的应用.
C、Be、Cl、Fe等元素及其化合物有重要的应用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com