
 某学生用邻苯二甲酸氢钾(相对分子质量为204)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol/L左右,滴定终点时溶液的pH约为9.1.
某学生用邻苯二甲酸氢钾(相对分子质量为204)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol/L左右,滴定终点时溶液的pH约为9.1.

| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4162 | 18.25 |
| 2 | 17.04 | |
| 3 | 16.96 |
 ;
; ;
;| m |
| M |
| 17.04+16.96 |
| 2 |
| n |
| V |


科目:高中化学 来源: 题型:阅读理解

 ,相对分子质量为204.0)是常用的基准物质.某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度.在本实验中达到滴定终点时,溶液的pH约为9.1.
,相对分子质量为204.0)是常用的基准物质.某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度.在本实验中达到滴定终点时,溶液的pH约为9.1.| 实验编号 | NaOH溶液的体积(mL) |
| 1 | 22.52 |
| 2 | 22.49 |
| 3 | 22.50 |
| ||
(
|
| ||
(
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 化学是一门以实验为基础的自然科学,
化学是一门以实验为基础的自然科学,
化学实验在化学学习中具有重要的作用。
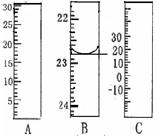
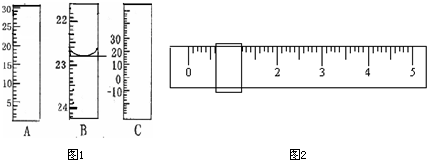
右图分别是温度计、量筒、滴定管的一部分,
其中A仪器的名称为 ,
B的正确读数为 。
(2)实验室很难配制准确浓度的NaOH溶液,需要
![]() 用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
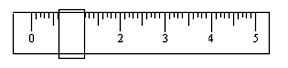 ①该学生用托盘天平称量时,先在两边托盘上放等质量的纸片,取少量邻苯二甲酸氢钾置于左盘,只用游码(单位:g)调整平衡时如下图所示。由此可知,所取邻苯二甲酸氢钾的质量为 g。
①该学生用托盘天平称量时,先在两边托盘上放等质量的纸片,取少量邻苯二甲酸氢钾置于左盘,只用游码(单位:g)调整平衡时如下图所示。由此可知,所取邻苯二甲酸氢钾的质量为 g。
②将称好的邻苯二甲酸氢钾置于锥形瓶中,加适量蒸馏水完全溶解得到无色溶液,再加入1~2滴 指示剂,当观察到 现象时,可停止滴定,记录数据。
③该学生进行了三次实验,所取固体质量均相同,达到滴定终点时记录所用未知氢氧化钠溶液的体积如下表:
| 实验编号 | NaOH溶液的体积(mL) |
| 1 | 22.52 |
| 2 | 22.49 |
| 3 | 22.50 |
则计算氢氧化钠溶液物质的量浓度的表达式为: (用数据表示,不需计算)
④以下操作会造成NaOH溶液浓度偏高的是 (填序号)
A.未用氢氧化钠溶液洗涤碱式滴定管
B.滴定前平视,滴定后俯视读数
C.滴定前滴定管尖嘴有气泡,滴定后气泡消失
D.滴定前未用邻苯二甲酸氢钾溶液洗锥形瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用邻苯二甲酸氢钾![]() ,式量为204.0)测定NaOH溶液的浓度,若每次都精确取用邻苯二甲酸氢钾为0.2040g.滴定终点时溶液的pH约为9.1(pH计测量),滴定时用酚酞做指示剂,用待测NaOH溶液滴定邻苯二甲酸氢钾,该生进行三次实验,每次消耗氢氧化钠溶液的体积如下表!
,式量为204.0)测定NaOH溶液的浓度,若每次都精确取用邻苯二甲酸氢钾为0.2040g.滴定终点时溶液的pH约为9.1(pH计测量),滴定时用酚酞做指示剂,用待测NaOH溶液滴定邻苯二甲酸氢钾,该生进行三次实验,每次消耗氢氧化钠溶液的体积如下表!
| 实验编号 | 邻苯二甲酸氢钾质量(g) | 待测NaOH溶液体积(mL) |
| l | 0.2040 | 23.20 |
| 2 | 0.2040 | 19.95 |
| 3 | 0.2040 | 20.05 |
(1)计算NaOH溶液的物质的量浓度
(2)该学生测定出来的NaOH溶液的物质的量浓度高于其实际值,造成该结果的原因可能是_________.
A.盛放邻苯二甲酸氢钾的锥形瓶未用待装液润洗
B.读消耗NaOH溶液的体积时,滴定前仰视,滴定后俯视
C.滴速太快没来得及观察就已经变色
D.配制NaOH溶液时,NaOH固体中可能混有KOH
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 实验编号 | NaOH溶液的体积(mL) |
| 1 | 22.52 |
| 2 | 22.49 |
| 3 | 22.50 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com