
下列物质在水溶液状态下电离方程式错误的是( )
A.CaCO3 = Ca2++CO32—
B.NaHSO4 = Na++HSO4—
C.H2CO3 H++HCO3—
H++HCO3—
D.NH3·H2O NH4++OH—
NH4++OH—
科目:高中化学 来源: 题型:
在含有FeBr2和FeI2的混合溶液中,通入过量的氯气,然后把溶液加热蒸干、灼烧,最后留下的是①FeCl2、②FeCl3、③I2、④Br2、⑤Fe(OH)3、⑥Fe2O3、⑦FeO。
A、①③④ B、③⑦ C、③⑤ D、⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M与X同主族,与W同周期。
(1)M元素是________(填元素符号)。
(2)Z、W形成的气态氢化物的稳定性为 > (填化学式)。
(3)M2Z2的电子式为________________,写出M2Z2与水反应的离子方程式:
。
(4)由X、Y、Z、W四种元素中的三种组成的—种强酸,该强酸的稀溶液能与铜反应,离子方程式为__________________________________________。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知:
①1 mol A能与足量NaOH浓溶液反应生成标准状况下44.8 L气体;
②A能与盐酸反应产生气体B,该气体能与氯水反应。
则A是____________(填化学式);写出该气体B与氯水反应的离子方程式:_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L的密闭容器中,发生以下反应:2A(g) + B(g) 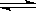 2C(g) + D(g)。若最初加入的A和B都是3 mol,在前10 s A的化学反应速率为0.12 mol/(L·s),则10 s时,容器中B的物质的量是( )
2C(g) + D(g)。若最初加入的A和B都是3 mol,在前10 s A的化学反应速率为0.12 mol/(L·s),则10 s时,容器中B的物质的量是( )
A.0.6 mol B.1.2 mol C.2.4 mol D.1.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 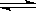 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
①N2O4的消耗速率与NO2的生成速率之比为1∶2;②NO2的生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A.②③⑥⑦ B.①④⑧ C.只有①④ D.只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中,反应aA(g) 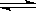 bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的160%,则( )
bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的160%,则( )
A.a>b B.物质A的转化率增大了
C.物质A的质量分数减小了 D.平衡向逆反应方向移动了
查看答案和解析>>
科目:高中化学 来源: 题型:
完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是( )
A.0.2Q B.0.1Q C.5Q D.10Q
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达平衡,平衡常数K=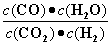 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为CO+H2O CO2+H2
CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com